Медицинская реабилитация
Передний доступ для стабилизации шейного отдела позвоночника
Д. Е. Яриков, А. В. Басков
НИИ нейрохирургии им. Н. Н. Бурденко, 19 городская клиническая больница, Москва
Статья рассчитана на начинающих нейрохирургов и травматологов, занимающихся лечением заболеваний позвоночника. Кратко дается история вопроса. Подробно разбирается техника переднего доступа к С3-T1 позвонкам, способы установки трансплантата и стабилизирующих пластин. Представлены данные литературы и собственный материал авторов, касающийся результатов и осложнений стабилизирующих операций на нижнешейном отделе позвоночника передним доступом.
Введение
Передний доступ для декомпрессии спинного мозга и стабилизации шейного отдела позвоночника был впервые предложен Leroy и Abott в Мичиганском университете, США, и первая операция была выполнена хирургами того же университета R. W. Bailey и С. Е. Badgley в 1952 году [8]. В 60-е годы передний подход для лечения травматических, дегенеративных, опухолевых и инфекционных поражений шейного отдела позвоночника получил широкое распространение в Северной Америке и Западной Европе благодаря работам G. W. Smith и R. A. Robinson - 1958, R. D. Cloward - 1961, H. Verbeist - 1969 [15, 32, 38]. В нашей стране этот доступ пропагандировали и развивали А. А. Луцик, А. И. Осна, Я. Л. Цивьян, Г. С. Юмашев [1-5].
Показанием для операций передним доступом на шейном отделе позвоночника являются заболевания, приводящие к его нестабильности за счет поражения передних опорных структур позвоночного столба (тел позвонков, межпозвонковых дисков, передней и задней продольной связки). Нестабильность может развиться вследствие травмы, дегенеративных поражений, опухоли, инфекции.
Процент успешных операций при дегенеративном поражении позвоночника, когда замещается один межпозвонковый диск, достаточно высок и составляет 74-98%, при этом миграция трансплантата отмечается в 2,1-4,6%. При вариантах травмы, которые сопровождаются повреждением заднего связочного аппарата, при необходимости замещения тела позвонка, фиксация одним трансплантатом потенциально нестабильна. В этих случаях смещение трансплантата отмечается в 29-68% случаев, консолидация не наступает у 33% больных, кифоз в позднем периоде травмы развился в 38-64% случаев.
Причинами подобных осложнений были [7, 19, 37]:
- необнаружение нестабильности задних структур;
- несовершенная техника установки трансплантата;
- неадекватная внешняя иммобилизация после операции.
Чтобы избежать этих осложнений, предлагают или комбинированные доступы - передний и задний спондилодез, или применение передних пластин.
Впервые металлическая пластина с винтами для дополнительной фиксации шейного отдела позвоночника при переднем доступе была использована J. ВоЫег в 1964 году, и результаты были опубликованы в Германии тремя годами позже [9]. Затем D. Orozco и соавт. [29] в 1970 и W. Caspar и соавт. [13] в начале 80-х предложили свои системы, которые и получили наиболее широкое распространение. Винты в этих конструкциях в самой пластине не закреплялись и для прочной фиксации должны были проводиться через два кортикальных слоя позвонка, что увеличивало риск повреждений спинного мозга и корешков. Кроме того, конструкция изготавливалась из стали, и после ее установки невозможно было произвести МР-томографию.
Е. Morsher и соавт. [27] разработали стабилизирующую систему, в которой винты фиксируются в самой пластине и имеют блокировку от раскручивания. Это усиливает стабилизацию, придает конструкции дополнительную прочность и безопасность. Поскольку при использовании этих пластин не было необходимости проводить винты через два кортикальных слоя позвонка, их назвали монокортикальными, в отличие от предыдущих, бикорти-кальных. Они изготовлялись из титана и были МРТ-совместимыми.
Недостатком этих пластин является заданное направление винтов, что может создавать трудности, когда требуется ввести винт под другим углом, чтобы избежать, например, его проникновения в межпозвонковый диск.
В последние 2 года начали выпускать универсальные системы, где винты и блокируются, и могут быть введены под различными углами.
За счет использования передних пластин достигается:
- Устранение деформации и поддержание правильной оси позвоночника.
- Обеспечение немедленной послеоперационной стабильности.
- Снижение вероятности смещения трансплантата в раннем послеоперационном периоде.
- Увеличение вероятности образования костного блока.
- Уменьшение необходимости в наружной иммобилизации.
Показанием к установке пластин является:
- Корпородез после удаления одного или двух тел позвонков.
- Корпородез после удаления травматической грыжи межпозвонкового диска, когда имеется нестабильность задних опорных структур (как альтернатива дополнительной стабилизации задним доступом).
- Удаление двух межпозвонковых дисков.
- Подвижность трансплантата после удаления одного диска при дегенеративном поражении позвоночника.
За последние 2 года в отделении хирургии позвоночника и спинного мозга 19 городской клинической больницы г. Москвы произведено 88 операций передним доступом на шейном отделе позвоночника. Стабилизацию производили ауто-трансплантатом из гребня подвздошной кости, в 80 случаях ее дополняли передней пластиной. Мы используем практически все выпускаемые в настоящее время конструкции ("Орион" США, "Кодман" США, "Матис" Швейцария).
Техника операции передним доступом на уровне С3-T1 позвонков
Пациент находится в положении на спине, под плечи подкладывают небольшой валик, плечи отводят вниз и фиксируют. При нестабильных повреждениях, когда требуется иммобилизация или устранение деформации оси позвоночника, применяют скелетное вытяжение. Мы чаще используем вытяжение за скуловые дуги.
Наружными анатомическими ориентирами для определения места разреза в зависимости от уровня поврежденного позвонка являются:
Таблица 1
| Уровень поврежденного позвонка | Анатомическая структура (ориентир для разреза) |
|---|---|
| С3 | Подъязычная кость |
| С4-С5 | Щитовидный хрящ |
| С6 | Перстневидный хрящ |
| C7-T1 | Надключичный уровень |
Для контроля за уровнем вмешательства производят рентгенографию шейного отдела позвоночника в боковой проекции.
Хирург и ассистент располагаются друг напротив друга по обе стороны от шеи больного. Хирург находится на стороне разреза. Для хирурга-правши удобнее делать разрез справа, но в этом случае появляется вероятность повреждения возвратного нерва. Поэтому при операциях на уровне С2-С5 мы осуществляем доступ справа, при операции на нижележащих позвонках - слева.
Выбор разреза зависит от количества позвонков, к которым осуществляется доступ. Для обнажения одного диска на любом уровне или двух тел позвонков на уровне С5-Т1 достаточно поперечного разреза, проводимого по естественным складкам шеи. Послеоперационный рубец от такого разреза менее заметен. Этот доступ позволяет не пересекать m.omohyoideus.
Для доступа к С2-С4 позвонкам или при необходимости обнажить три тела позвонка производят разрез по переднему краю m.sternocleidomastoideus.
Разрезают кожу с подкожной клетчаткой. Затем рассекают платизму. Обнажается внутренний край m.sternodeidomastoideus. По ее внутреннему краю часто проходит довольно крупная вена, соединяющая переднюю яремную вену с лицевой. В большинстве случаев эту вену удается отвести, но при необходимости она может быть коагулирована. Иногда эта вена может быть очень крупной - диаметр ее может достигать 1 см. В этом случае внутренняя яремная вена имеет небольшой диаметр. Поэтому препаровка переднего края m.sternodeidomastoideus должна проводиться осторожно.
Фасцию, окружающую кивательную мышцу, рассекают по переднему краю.
Под m.sternodeidomastoideus располагается верхнее брюшко т. omohyoideus, идущее в косом направлении сверху вниз и изнутри кнаружи. Инсгда мышцу возможно отвести вверх или вниз, но чаще всего, особенно при операциях с обнажением трех и более тел позвонков, ее пересекают. Для этого под мышцу вводят москит, мышцу выделяют на протяжении 1,5-2 см, под нее проводят две лигатуры, мышцу перевязывают и пересекают. В дальнейшем мышца может быть сшита, но и не сшивание ее не приводит к каким-либо функциональным потерям.
М. omohyoideus прилежит к фасции, окружающей сосудисто-нервный пучок, состоящий из медиально лежащей общей сонной артерии, яремной вены и блуждающего нерва. Пучок отводят латерально, пальцем нащупывают переднюю поверхность тел позвонков. Этот момент важен, поскольку он позволяет ориентироваться в дальнейшем направлении доступа, чтобы не выйти слишком латерально на длинные мышцы шеи. Удобно сделать несколько продольных движений тупфером над телами позвонков в направлении оси позвонсн-ника. Это позволит разъединить претрахеальную фасцию, окружающую щитовидную железу, пищевод и трахею от фасции, окружающей сосудисто-нервный пучок, лучше рассмотреть его и оттеснить латеральнее. Сосудисто-нервный пучок и гортань с пищеводом разводят зеркалами или крючками Фарабефа в стороны. Ножницами и тупфером разъединяют фасцию, окружающую сосудисто-нервный пучок. При этом необходимо всегда ориентироваться, где находится сонная артерия. На уровне С4 позвонка и выше, Q позвонка и ниже могут встретиться соответственно верхняя и нижняя щитовидные артерии. Их необходимо аккуратно выделить вместе с сопровождающими их венами и, если они мешают доступу, перевязать и пересечь.
После этого фасцию раздвигают в продольном направлении. Становится вцдна передняя поверхность тел позвонков, межпозвонковые диски. Над ними находится превертебральная фасция, которую мы предпочитаем раздвигать тупо, тупфером, иногда пользуясь ножницами, при необходимости коагулируя имеющиеся в ней мелкие сосуды. Ассистент должен с определенным усилием отодвигать гортань, чтобы хирург имел возможность видеть переднюю поверхность тел позвонков. Необходимо четко видеть оба внутренних края m. longus coli с двух сторон, поскольку это позволяет ориентироваться относительно центра позвонков. При рассечении превертебральной фасции необходимо помнить, что над телами позвонков находится пищевод, который должен быть отведен.
После того, как передняя поверхность тел позвонков обнажена, в межпозвонковый диск или тело позвонка, в зависимости от объема операции, вводят иглу и осуществляют рентгеновский контроль уровня операции. Затем коагулируют внутренние края длинных мышц шеи, их отодвигают распатором и под них вводятся зеркала ретракторов. Скальпелем по краю тел позвонков рассекают фиброзные кольца. По границам удаляемых межпозвонковых дисков их фиброзные кольца отделяют скальпелем от тел позвонков на ширину приблизительно 10-15 мм. При этом мы пользуемся узким скальпелем, не погружая его в диск больше чем на 10 мм. Затем конхотомом удаляют межпозвонковые диски. Для того, чтобы диск был удален полностью, следует ориентироваться на поверхность унковертебральных сочленений. При этом латеральные порции дисков можно удалить ложкой небольших размеров. Делать это нужно осторожно, чтобы не повредить корешки спинного мозга. Когда диск удален полностью, у хирурга возникает ощущение, что инструмент упирается и скребет кость.
Для удаления тела позвонка мы используем бор с круглой фрезой диаметром 5-6 мм. Как только бор доходит до задней продольной связки, она обнажается на небольшом участке, и дальнейшее удаление производят пистолетными кусачками с толщиной основания 2 мм.
Удаляя тело позвонка, следует всегда помнить, что межпозвонковые диски располагаются не перпендикулярно к дуральному мешку, а идут под углом 10-15 градусов спереди назад. Поэтому, если с нижним краем удаляемого позвонка и прилегающим диском обычно не бывает проблем, то при удалении верхнего диска и верхнего края позвонка надо строго проследить, чтобы была полностью удалена задне-верхняя часть тела с прилегающим участком диска (см. рис. 1, а). В противном случае не будет достигнута адекватная декомпрессия дурального мешка, а при установке трансплантата неуцаленный фрагмент диска и позвонка могут быть смещены в позвоночный канал и вызвать компрессию спинного мозга и неврологические нарушения. Удалять эту часть позвонка лучше всего тонкими пистолетными кусачками.
Нижнюю замыкательную пластинку вышележащего позвонка и верхнюю замыкательную пластинку нижележащего позвонка осторожно, обычно с помощью острых ложек, освобождают от хряща, не повреждая субхондральный слой. При удалении субхондрального слоя не следует повреждать его до губчатой кости - трансплантат может продавливать тела позвонков.
Удаленное тело позвонка может быть замещено аутотрансплантатом из гребня подвздошной кости, аллотрансплантатом из малоберцовой кости, имп-лантатом из никелцда титана, керамики. Мы предпочитаем трансплантат из гребня подвздошной кости, дополняя его в случае необходимости передней пластиной. При взятии трансплантата из передней части гребня подвздошной кости возможно повредить n.cutaneus femoralis lateralis, который обычно проходит впереди передней верхней подвздошной кости, но может иметь варианты прохождения. Повреждение нерва может привести к хронической боли и потере чувствительности на боковой поверхности бедра. Для того, чтобы избежать этого осложнения, желательно не брать трансплантат ближе чем на 2 см к передней верхней подвздошной кости.
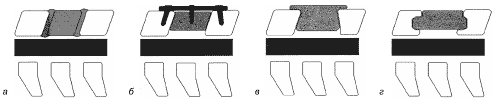
Рис. 1. а - серым цветом выделено тело позвонка и межпозвонковые диски, подлежащие удалению. Заштрихован фрагмент тела позвонка и диска, который может быть не удален, если не учтено наклонное расположение тел позвонков и межпозвонковых дисков; б - установлен трансплантат, стороны которого смоделированы по направлению тел и выше-, и нижележащих позвонков. Трансплантат фиксирован пластиной и дополнительным винтом, в - Варианты трансплантатов из гребня подвздошной кости, устанавливаемых без пластин. В случае в гребень подвздошной кости располагается сверху, в случае г снизу. В случае г также может быть использован аллотрансплантат из малоберцовой кости.
Форма трансплантата зависит от того, будет ли установлена передняя фиксирующая пластина или нет. Если ее не устанавливают, то в телах позвонков формируют пазы для установки трансплантата и самому трансплантату прцдают форму, соответствующую пазам (см. рис 1, в и г).
Если трансплантат будут укреплять пластиной, то ему придают форму параллелепипеда, с углами 10-15°, соответствующими углу наклона межпозвонковых дисков. При этом удается достичь максимальной поверхности соприкосновения трансплантата и позвонков.
Перед установкой трансплантата дистрактором увеличивают промежуток между позвонками, в который будет установлен трансплантат, что позволит установить трансплантат без излишних усилий. Мы предпочитаем дистрактор Каспара, имеющий спицы с резьбой и ограничителем. Спицы вводят в тела выше- и нижележащих позвонков и они не мешают установке трансплантата. Мы использовали и другие дистракторы с лапками, упирающимися в замыкательные пластины позвонков, медду которыми устанавливают трансплантат, но они с нашей точки зрения менее удобны.
Следует избегать чрезмерного растяжения позвонков, поскольку это увеличивает нагрузку на соседние сегменты, может суживать межпозвонковые отверстия, приводить к переломам соседних тел позвонков, в которые введены спицы или упираются лапки дистрактора.
Легкое поколачивание по трансплантату во время его установки допустимо. Если дистрактора нет, возможно произвести дополнительную наружную тракцию. После установки трансплантата тракцию прекращают, вытяжение снимают.
Отдельные моменты техники установки пластин
Крайне важно удалить все мягкие ткани и переднюю продольную связку с передней поверхности тел позвонков. Очень часто при этом обнажаются невидимые до этого неровности передней поверхности, которые могут мешать установке пластины. Их надо удалить, не повреждая наружный кортикальный слой.
В шейных позвонках кость имеет максимальную плотность в соседней с замыкательными пластинами области. Поэтому желательно подбирать пластину такой длины, чтобы места ввинчивания шурупов приходились на эти зоны. Края пластины будут располагаться примерно на середине тел позвонков, в которые будут ввинчиваться винты. При этом место введения винтов должно отступать от края диска минимум на 2 мм (см. рис. 1, б; рис. 2, а, б, в).
Необходимо избегать введения винтов в межпозвонковый диск. Это уменьшает прочность их крепления, может приводить к миграции пластины, а также к быстрой дегенерации диска и возникновению болей в шее. Кроме того, пластина не должна заходить на интактные диски, так как в этом случае при сгибании шеи на края пластины будет оказываться давление. Поэтому винты следует устанавливать под контролем электронно-оптического преобразователя или делать контрольные снимки. Следует учитывать, что диски располагаются под углом от 10 до 20 градусов спереди назад, поэтому траектория винтов должна приблизительно соответствовать этому направлению. Этого трудно добиться при установке нижних винтов. Здесь можно расположить винты ближе к головному концу и, придав им перпендикулярное направление (если позволяет конструкция пластины), избежать попадания в диск. На установку нижних винтов следует обратить особое внимание, поскольку несостоятельными чаще оказываются они.
Послеоперационная иммобилизация
Сроки иммобилизации связаны со временем консолидации трансплантата. Хотя считается, что для полной консолидации требуется 8-12 месяцев, через 3 месяца образуется достаточно надежный костный блок. A. A. White и соавт. [39] полагают, что уже через 6 месяцев стабилизация достигает своей полной силы. Наиболее ответственный период приходится на первый месяц. Мы осуществляем послеоперационную иммобилизацию жестким воротником. При использовании пластин больному разрешается вставать на 2-3 сутки. Обычный срок ношения жесткого воротника 8-12 недель, затем в течение 1 месяца мы рекомендуем ношение мягкого воротника. Через полгода после операции может быть разрешена полная физическая активность. Безусловно, необходимо учитывать конкретную хирургическую ситуацию, характер операции, рентгенологические данные, активность пациента. Рентгеновский контроль мы проводим сразу после операции, через 2 недели, а затем через 1,3, 6 и 12 месяцев после операции.
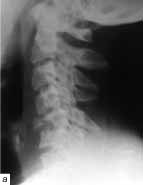
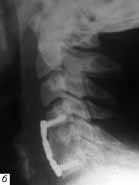
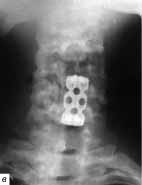
Рис. 2. а - компрессионный перелом С3 позвонка. Тело С3 позвонка фрагментировано, его задне-нижний край внедряется в позвоночный канал; б и в - тело С3 удалено и заменено трансплантатом из гребня подвздошной кости. Установлена фиксирующая пластина, винты введены в тела С4 и С6 позвонков.
Осложнения при операциях передним доступом
Ниже приведен список возможных осложнений при операции передним доступом, а также данные литературы и наши собственные данные о частоте их встречаемости.
Таблица 2
| Осложнения | Частота встречаемости | |
|---|---|---|
| по данным литературы | анализ собственных наблюдений (86) | |
| Повреждение нервных структур позвоночного канала | ||
| Спинного мозга | 0 до 2,1% [30, 40] |
1,2% |
| Нервных корешков | 0% | |
| Твердой мозговой оболочки | 2,3% | |
| Повреждения сосудов | ||
| Сонной артерии | 0% | |
| Внутренней яремной вены | 0% | |
| Позвоночной артерии | 0% | |
| Повреждение возвратного нерва | 1-11% [12, 22, 34] | 0% |
| Повреждение пищевода | 0,2-1,33% [11, 35] | 1,2% |
| Повреждение трахеи | 0% | |
| Синдром Горнера | Менее 1% [19] | 0% |
| Повреждение грудного лимфатического протока | 1,33% [10] | 0% |
| Пневмоторакс | 0% | |
| Осложнения в месте взятия трансплантата | ||
| Гематома | 9% [17] | 0% |
| Стойкие боли в месте взятия трансплантата | 12%-37% [16, 17, 20] |
|
| Анестезия, гиперестезия, хроническая боль по боковой поверхности бедра | 2,66% [33] | 0% |
| Воспаление раны на шее | 1% [34] | 1,2% |
| Гематома послеоперационной раны | 9% [30] | 0% |
| Подкожное скопление ликвора при повреждении твердой мозговой оболочки | 2,3% | |
Результаты применения передних пластин
Данные литературы демонстрируют значительное увеличение (до 100% [25]) надежности спонди-лодеза без дополнительной задней фиксации за счет применения передних пластин при крайне нестабильных вариантах травмы шейного отдела позвоночника [6, 21]. При этом раневая инфекция, неврологические осложнения и повреждения пищевода встречаются в таком же проценте случаев, как и при установке трансплантата без пластины [28].
М. A. Eleraky и соавт. [18] представили результаты 185 операций передним доступом при дегенеративных процессах, травмах, опухолях, инфекции, кифозе шейного отдела позвоночника. 70 пациентам производилось удаление тел 2 позвонков, 87 - одного, 28 - трех. Аутотрансплантат из гребня подвздошной кости использован в 141 случае, аллотрансплантат из малоберцовой кости - в 44. В 179 случаях применялись передние пластины. Послеоперационной летальности не отмечено. Также не было стойких неврологических осложнений. Осиплость голоса, дисфагия и боль в области взятия трансплантата имели преходящий характер. Прочный костный блок получен у 98,8% больных. V. Heidecke и соавт. [23] проанализировали 96 случаев операций по поводу травм, опухолей, остеомиелита и дегенеративных поражений шейного отдела позвоночника с использованием передних пластин.
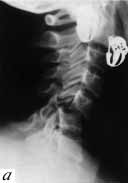
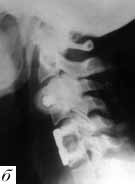
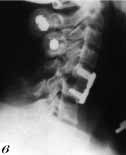
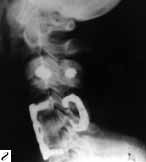
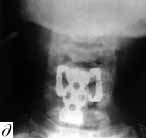
Рис. 3. а - вывих С5 позвонка; б - состояние после первой операции. Произведена стабилизация на уровне С5-С6 позвонков аутотрансплантатом и пластиной "Кодман"; в - контрольная рентгенограмма после повторной травмы. Имеется кифоз и перелом С6 позвонка, в который были установлены нижние винты; г и д - боковая и передняя рентгенограммы после повторной одномоментной комбинированной стабилизации перелома передней пластиной системы "Кодман" и задней стабилизации системой "Апофикс".
Во всех случаях достигнут надежный костный блок. В трех случаях наблюдалось смещение пластин, которое было связано с ошибками при их установке. G. L. Lowery и R. F. McDonough [26] рассмотрели частоту поломок передних пластин у 109 пациентов с дегенеративным поражением позвоночника. 70 пациентам бьши установлены бикортикальные пластины, без блокировки винтов, 39 - мснокор-тикальные, с блокировкой. Время наблюдения составило в среднем 43 месяца. Поломка пластины или винта определялась независимо от клинического значения. Было выявлено 32 поломки бикор-тикальных и 7 поломок монокортикальных пластин. Ни в одном случае не было отмечено повреждения сосудисто-нервного пучка, трахеи или пищевода. Дальнейшего смещения пластины или винтов в большинстве случаев не наблюдалось. Авторы считают, что поломка пластин чаще всего связана с несращением перелома. Немедленное удаление пластин необходимо редко. Оно показано при нарастании кифоза и повторном вмешательстве вследствие его.
При нестабильных вариантах травмы, когда имеется поражение всех опорных структур позвоночника или поражение позвоночника на нескольких уровнях, применение пластин не может гарантировать его стабильность.
A. R. Vaccaro и соавт. [36] проанализировали ранние осложнения стабилизации позвоночника передними пластинами после корпородеза на уровне двух и трех позвонков у больных с травмами, опухолями и дегенеративными заболеваниями. В раннем послеоперационном периоде смещение трансплантата и конструкции отмечено у 3 из 33 больных, которым произведено удаление двух тел позвонков (9%), и у 6 из 12 (50%), оперированных на трех уровнях. Авторы считают, что стабилизация только передними пластинами при операции на трех уровнях не обеспечивает адекватной стабильности, независимо от способа наружной фиксации.
У 79 из 80 пациентов мы использовали монокортикальные пластины. Смещение пластины наблюдалось только в одном случае, после повторной травмы (рис. 3, а, б, в, г, д). Больной по поводу вывиха С5-C6 позвонков и травматической грыжи межпозвонкового диска с компрессией дурального мешка была произведена стабилизация на уровне С5-C6 позвонков аутотрансплантатом и пластиной "Кодман". Через месяц после выписки больная упала, ударившись лбом. Во время удара ощутила "хруст" и боль в шее, боли в руках. При контрольной рентгенографии выявлено нарастание кифоза и перелом позвонка, в который были установлены нижние винты. Нарастания неврологических нарушений не отмечено. Произведена одномоментная комбинированная стабилизация перелома передней пластиной системы "Кодман" и задняя стабилизация системой "Апофикс". Больная выписана из отделения через 20 дней после операции без неврологического дефицита. На контрольных рентгенограммах через 1 и 3 месяца после травмы положение имплантатов правильное.
Заключение
Операции на шейном отделе позвоночника передним доступом производят уже более 40 лет. Внедрение современных средств фиксации позволяет повысить надежность спондилодеза и в ряде случаев избежать необходимости дополнительной стабилизации задним доступом. Установка стабилизирующих пластин требует от хирурга определенной подготовки. Необходимо также учитывать экономический фактор, поскольку стоимость стабилизирующих конструкций оплачивает пациент. После удаления трех тел позвонков, надежной стабилизации позвоночника только через передний доступ достичь трудно, даже при применении средств внутренней фиксации.
Основой надежной стабилизации является не применение какой-либо конструкции, а правильная установка межтелового трансплантата с последующим образованием надежного костного блока. Средства внутренней фиксации являются только вспомогательными. Главное, что определяет успех операции, это правильная оценка нестабильности повреждения, адекватная хирургическая тактика, тщательная подготовка ложа трансплантата и подбор его размеров, надежная послеоперационная иммобилизация.
Литература
Луцик А. А. // Позвоночно-спинномозговая травма (диагностика, лечение, реабилитация): Сб. трудов, кафедры нейрохирургии. - Новокузнецк, 1988. - С. 84-96.
Луцик А. А. II В кн.: Травма шейного отдела позвоночника и спинного мозга. - Ленинград, 1981. - С. 33-36.
Осна А. И. II Сб. Травма шейного отдела позвоночника и спинного мозга. - Ленинград, 1981. - С. 18-22
Цивъян Я. Л. Лечение застарелых повреждений средне- и нижнешейного отделов позвоночника: Методические рекомендации. - Новосибирск, 1982.
Юмашев Г. С., Фурман М. Е. Остеохондрозы позвоночника. 2-е изд. - М: Медицина, 1984. - 384 с.
Aebi M, Zuber К, Marchesi D. Treatment of cervical spine injuries with anterior plating: indications, techniques, and results // Spine. - 1991. - Vol. 16 (3S). - P. 38-45.
Abitbol J. J. Anterior Cervical Plating. 4th International Neu-rotrauma Symposium. Satellite Symposium II. Spinal Instrumentation. August 23, Seoul., Korea 1997. - P. 29-32.
Bailey R. W., Badgley С. Е. Stabilization of the cervical spine by anterior fusion // J. Bone Joint Surg. [Am.]. - 1960. - Vol. 42A. - P. 565-594.
Bohler J. Sofort- und Fruhbehandlung traumatisher Querschnit-tlahmungen // Z. Orthop. - 1967. - Vol. 103. - P. 512-528.
Bohlmann H. H. Acute fractures and dislocations of the cervical spine. An analysis of three-hundred hospitalized patients and review of the literature // J. Bone Joint Surg. - 1979. - Vol. 61(A). - P. 1119-1142.
Bohlmann H. H., Eismont F. J. Surgical techniques of anterior decompression and fusion for spinal cord injuries // Clin. Orthop. - 1981. - Vol. 154. - P. 57-67.
Bulger R. F., Rejowski J. E., Beatty R. A. Vocal cord paralysis associated with anterior cervical fusion. Consideration for prevention and treatment // J. Neurosurg. - 1985. - Vol. 62. - P. 657-661.
Caspar W. Advances in cervical spine surgery: First experiences with the trapezial osteosynthetic plate and a new surgical instrumentation for anterior interbody stabilization // Orthop. News. - 1982. - Vol. 4. - P. 7-8.
Caspar W., Barbier D. D., Klara P. M. Anterior cervical fusion and Caspar plate stabilization for cervical trauma // Neurosur-gery. _ 1989. _ Vol. 25. - P. 491-502.
С toward R. D. Treatment of acute fractures and fractures dislocations of the cervical spine by vertebral body fusion // J. Neurosurg. - 1961. - Vol. 18. - P. 205-209.
Dawson E. G., Lotysch M., Urist M. R. Intertransverse process lumbar arthrodesis with autologous bone graft // Clin. Orthop. - 1981. - Vol. 154. - P. 90-96.
DePalma A., Rothman R. H., Lewinnek G., Canale S. Anterior interbody fusion for severe cervical disc degeneration // Surg. Gynecol. Obstet. - 1972. - Vol. 134. - P. 755-758.
Eleraky M. A., Llanos C., Sonntag V. K. Cervical corpectomy: report of 185 cases and review of the literature // J. Neurosurg. - 1999. - Vol. 90 (1 Suppl), Jan. - P. 35-41.
Flynn Т. В. Neurologic complications of anterior cervical interbody fusion // Spine. - 1982. - Vol. 7. - P. 536-539.
Frymoyer J. W., Howel J., Kuhlman D. The long-term effects of spinal fusion on the sacroiliac joints and ilium // Clin. Orthop. - 1978. - Vol. 134. - P. 196-201.
Garvey T. A., Eismont F. J., Roberti L. J. Anterior decompression, structural bone grafting, and Caspar plate stabilization for unstable cervical spine fractures and/or dislocations // Spine. - 1992. - Vol. 17, N 10. - P. 431-435.
Heeneman H. Vocal cord paralysis following approaches to the anterior cervical spine // Laryngoscope. - 1973. - Vol. 83. - P. 17-21.
Heidecke V., Rainov N. G., Burkert W. Anterior cervical fusion with the Orion locking plate system // Spine. - 1998. - Vol. 23, N 16, Aug 15. - P. 1796-1802; discussion P. 1803.
Horwitz N. H., Rizzoli M. V. Postoperative Complications in Neurosurgery Practice, Recognition, Prevention, Management, Baltimore: Williams and Wilkins, 1988.
Krag M. H. Biomechanics of the Cervical Spine. In: The Adult Spine. Principles and Practice. Second Edition. Editor in chief John W. Frymoyer. 2nd ed. 1997, - Vol. 1. - P. 1075-1095.
Lowery G. L., McDonough R. F. The significance of hardware failure in anterior cervical plate fixation. Patients with 2- to 7-year follow-up // Spine. - 1998. - Vol. 23, N 2, Jan 15. -P. 181-186; discussion P. 186-187.
Morsher E., Sutler F., Jennis M., Olerud S. Die vordere Ver-plauting der HalswirbelsAule mit dem Hohlschrauben-Platten-system // Chirurg. - 1986. - Vol. 57. - P. 702-707.
Newhouse K. E., Lindsey R. W., Clark C. R., Lieponis J., Murphy M. J. Esophageal perforation following anterior cervical spine surgery // Spine. - 1989. - Vol. 14. - P. 1051-1053.
Orozco D., Llovet-Tapies J. Osteosintesis en las fractures de raquis cervical //Revista Orthop. Traumatol. - 1970. - Vol. 14. - P. 285-288.
Simeone F. A., Rothman R. H. Cervical disc disease. In: Rothman R. H., Simeone F. A. (eds) The Spine, 440-499. Philadelphia: WB Saunders, 1982.
Simmons E. H. The surgical correction of flexion deformity of the cervical spine in ankylosing spondylitis. In: Sherk H. H., Dunn E. J., Eismont F. J., et al. The Cervical Spine, 2nd ed, 573-598. Cervical Spine Research Society. Philadelphia: JB Lippincott, 1989.
Smith G. W., Robinson R. A. Treatment of certain cervical spine disorders by anterior removal of the intervertebral disc and interbody fusion // J. Bone Joint Surg. [Am.]. - 1958. - Vol. 40A. - P. 607-623.
Stauffer E. S., Coventry M. G. Anterior interbody lumbar spine fusion // J. Bone Joint Surg. [Am.]. - 1972. - Vol. 54. - P. 765-768.
Tew J. M., May field F. H. Complications of surgery of the anterior cervical spine // Clin. Neurol. - 1975. - Vol. 23. - P. 424-434.
Tew J. M., May field F. H. Surgery of the anterior cervical spine: preventions of complications. In: Dunsker SB (ed) Cervical Spondylosis, 191-208. New York: Raven Press, 1981.
Vaccaro A. R., Falatyn S. P., Flanders A. E., Balderston R. A., Northrup B. E., Cotler J. M. Magnetic resonance evaluation of the intervertebral disc, spinal ligaments, and spinal cord before and after closed traction reduction of cervical spine dislocations // Spine. - 1999. - Vol. 24, N 12, Jun. 15. -P. 1210-1217.
Van Peteghem P. K., Schweigel J. F. The fractured cervical spine rendered unstable by anterior cervical fusion // J. Trauma. - 1979. - Vol. 19. - P. 110-114.
Verbeist H. Anterolateral operations for fractures and dislocations in the middle and lower parts of the cervical spine // J. Bone Joint Surg. [Am.]. - 1969. - Vol. 18. - P. 205-209.
White A. A., Punjabi M. M., Tech D. The Role of Stabilization in the Treatment of Cervical Spine Injuries // Spine. - 1984. - Vol. 9, N 5. - P. 512-522.
Yonenobu K., Hosono N., Iwasaki M., Asano M., Ono K. Neurologic complications of surgery for cervical compression my-elopathy // Spine. - 1991. - Vol. 16. - P. 1277-1282.