Профилактика
Глава 4. Реабилитация после перенесенного инфаркта миокарда
Реабилитация после перенесенного инфаркта миокарда включает в себя следующие моменты.
1. Диета.
2. Лекарственная реабилитация (коррекция дислипидемий, возможных осложнений).
3. Дозированные физические нагрузки.
4. Лечебная гимнастика.
5. Психологическая реабилитация.
Под кардиологической реабилитацией понимают комплекс мероприятий, проводимых под медицинским руководством (контролем), направленных на помощь пациенту, который перенес инфаркт миокарда или тяжелое кардиологическое заболевание, а также после кардиохирургической операции, для более качественного и быстрого восстановления физических параметров до максимально возможного уровня активности. Помимо этого, этими мероприятиями необходимо обеспечить достоверное уменьшение риска повторных сердечных приступов и других сердечно-сосудистых нарушений, а также снижение вероятности ухудшения функционального состояния сердца.
Еще одним очень важным направлением реабилитации в кардиологии является психологическая реабилитация. Она направлена на положительный настрой пациента, улучшение восприятия им действительности после перенесенного инфаркта миокарда, а также на психологическую помощь в его намерении изменить свой образ жизни. Данное направление в реабилитации имеет очень большое значение для повышения выживаемости пациентов, которые перенесли инфаркт миокарда.
Обычно программа реабилитации пациента начинается еще в стационаре с работы по восстановлению потерянных из-за болезни основных навыков (таких, как самостоятельное передвижение по палате, в ванную комнату, в туалет, выполнение гигиенических процедур и т. д.). После того как происходит выписка пациента из стационара, реабилитация продолжается в домашних условиях под наблюдением и контролем лечащего врача. Основная задача реабилитационных мероприятий – предупредить проблемы с сердцем в дальнейшем. Программа кардиологической реабилитации является индивидуальной для каждого пациента, и ее содержание и длительность определяются разнообразными факторами.
Польза кардиологической реабилитации в следующем: различные системы реабилитации больных инфарктом миокарда позволяют в большинстве случаев избежать инвалидности и возвратиться к нормальной трудовой деятельности, снижают риск повторных сердечных приступов и других сердечно-сосудистых событий, снижают вероятность повторных госпитализаций в связи с кардиологическими проблемами, снижают риск смерти от сердечных заболеваний, улучшают физические кондиции пациента, снижают потребность в лекарственных препаратах, снижают артериальное давление.
Системы реабилитации также уменьшают содержание в крови атерогенных (ведущих к появлению атеросклеротических бляшек в просвете сосудов) жиров: общего холестерина, липопротеидов низкой плотности и триглицеридов, снижают страх, тревогу и депрессию, замедляют прогрессирование атеросклероза, обеспечивают снижение массы тела, повышение качества жизни.
Проблема повышения эффективности лечения и реабилитации больных инфарктом миокарда (ИМ) становится одной из важнейших в современной кардиологии и имеет большое медицинское и социальное значение. В последние десятилетия характерна неблагоприятная динамика показателей сердечно-сосудистой патологии и смертности практически во всех странах мира, кроме того, 90% всей сосудистой смертности выпадает на ишемическую болезнь сердца (ИБС) и ишемическую болезнь мозга. Между тем, самой неблагоприятной в отношении выживаемости и смертности является группа лиц, которые перенесли ИМ. Основным направлением в лечении и реабилитации пациентов, перенесших ИМ, является использование лекарственных препаратов, немедикаментозных методов и комплекса санаторно-курортных факторов.
Если 10–15 лет назад диагноз инфаркт миокарда сразу переводил пациента в группу инвалидов, то сейчас благодаря качественно разработанной системе реабилитации большое количество пациентов возвращается к своей прежней работе, к обычной жизни.
Лечение инфаркта миокарда не заканчивается лечением в стационаре. После стационара необходим длительный, до полугода, период реабилитационных мероприятий. В этот период постепенно нарастает физическая нагрузка. После перенесенного инфаркта миокарда жизнь пациента полностью меняется. Такому пациенту необходимо помнить, что фармацевтические препараты ему придется принимать всю оставшуюся жизнь. Вредные привычки необходимо ликвидировать. Артериальное давление постоянно придется контролировать. Но жизнь продолжается и после инфаркта, жить можно практически полноценно, следовать рекомендациям врачей. Все мероприятия реабилитации проводятся дифференцированно, в зависимости от тяжести состояния больного, особенностей клинического течения болезни, а также сопутствующих заболеваний и патологических процессов. Программа реабилитации становится естественным продолжением госпитального (стационарного) лечения.
На стадии реабилитации ставятся следующие задачи:
1) физическая – восстановление до максимально возможного уровня функции сердечно-сосудистой системы и восстановление физической работоспособности больных. Необходимо добиваться адекватной реакции на физическую нагрузку, что достигается в среднем через 2–6 недель физических тренировок, которые развивают коллатеральное кровообращение;
2) психологическая – у больных, перенесших инфаркт миокарда, нередко развивается страх перед повторным инфарктом, поэтому необходима психологическая реадаптация больных. При этом может быть оправдано применение психотропных средств;
3) социальная реабилитация, или подготовка к самостоятельной жизни и производственной деятельности: больной после перенесенного инфаркта миокарда считается нетрудоспособным 4 месяца, затем его направляют на ВТЭК. 50% больных к этому времени возвращается к работе, т. е. трудоспособность практически полностью восстанавливается. Если возникают осложнения, то временно устанавливается группа инвалидности, обычно II, на 6-12 месяцев.
Большое значение имеет реабилитация (восстановление стабильного уровня здоровья и трудоспособности больного). Активность больного в постели – с первого дня, присаживание – со 2–4 дня, вставание и ходьба – на 7-11 дни.
Сроки и объем реабилитации подбираются строго индивидуально, после выписки больного из стационара она завершается в поликлинике или санатории.
В отделение реабилитации местных санаториев переводятся пациенты с I–III классами тяжести заболевания при удовлетворительной адаптации их к четвертой ступени двигательной активности.
Имеются противопоказания для направления больного, перенесшего инфаркт миокарда, в санаторий:
1) общие противопоказания для поступления больного в санаторий (острые инфекционные заболевания, психические и онкологические заболевания, венерические заболевания, болезни крови в острой стадии и стадии обострения);
2) недостаточность кровообращения ИВ стадии и выше;
3) тяжелые степени коронарной недостаточности;
4) рецидивирующее течение инфаркта миокарда;
5) тяжелые степени нарушения проводимости и сердечного ритма;
6) гипертоническая болезнь ИВ-III стадии;
7) аневризма сердца (острая или хроническая) с выявлениями недостаточности кровообращения выше I стадии;
8) аневризма аорты;
9) нарушение мозгового кровообращения в острой или подост-рой стадии;
10) рецидивирующие тромбоэмболические осложнения;
11) декомпенсированный сахарный диабет.
Диета
Главными целями реабилитации больных, перенесших инфаркт миокарда, на диспансерно-поликлиническом этапе являются завершение периода временной нетрудоспособности, восстановление утраченной работоспособности, проведение мероприятий по вторичной профилактике инфаркта миокарда. Рациональное лечебное питание имеет огромное значение в комплексе реабилитационных мероприятий после инфаркта миокарда. Диетотерапия дает возможность нормализовать или хотя бы уменьшить явления атерогенной дислипидопротеинемии, а, следовательно, эффективна как первичная профилактика повторного инфаркта миокарда. Одновременное применение гиполипидемических препаратов с началом диетотерапии рекомендуется только тогда, когда необходимо немедленно снизить уровень липидов плазмы у лиц с генетически обусловленной резко выраженной дислипидемией и высоким риском развития ишемической болезни сердца или панкреатита (при высокой гипертриглицеридемии).
В 1987 г. группой экспертов по изучению атеросклероза сформулировано 7 «золотых правил» диеты, соблюдение которых поможет устранить нарушения обмена липопротеинов:
1) сократить употребление жиров;
2) резко уменьшить употребление продуктов, содержащих насыщенные жирные кислоты (животные жиры, сливочное масло, сливки, яйца), так как они способствуют гиперлипидемии;
3) увеличить потребление полиненасыщенных жирных кислот, которые содержатся в следующих продуктах: жидкие растительные масла, рыба, птица, морские продукты, полиненасыщенные жирные кислоты снижают уровень липидов в крови;
4) необходимо увеличить употребление клетчатки и сложных углеводов (овощи и фрукты);
5) полностью заменить при приготовлении пищи сливочное масло растительным маслом;
6) резко снизить употребление продуктов, богатых холестерином;
7) ограничить количество поваренной соли в пище до 3–5 г в сутки.
Данным условиям соответствует диета № 10, разработанная институтом питания РАМН.
Общая характеристика диеты включает следующие положения: нормальное содержание белка, ограничение жира (преимущественно животного), углеводов (преимущественно простых), поваренной соли (до 3–5 г в сутки), обогащение питания полиненасыщенными жирными кислотами за счет растительного жира, пищевыми волокнами, липотропными веществами и ограничение содержания холестерина.
Химический состав данной диеты характеризуется содержанием белков – 80–90 г (из них 60% животных), жиров -70 г (из них 1β растительных), углеводов – 350–400 г (из них 30 г представлены простыми углеводами), энергетическая ценность – 2300 ккал. Количество жидкости, потребляемой больным в течение суток, составляет 1,2 л, включая суп, компот, кисель и т. д.
Большое значение в диетотерапии приобретает витаминный состав пищевых продуктов, особенно важно содержание в них витаминов А, С, Д. Обоснованием повышенной витаминизации пищи является влияние указанных витаминов на процессы метаболизма миокарда и увеличение их потребления при инфаркте миокарда. Увеличение количества водорастворимых витаминов достигается широким включением в рацион свежих овощей и фруктов, преимущественное использование некоторых крупяных изделий (гречневая, овсяная каша), ряда мясных продуктов (телятина) и т. д., повышенная витаминизация жирорастворимыми витаминами осуществляется за счет включения в рацион оптимального количества жира растительного происхождения.
В нарушении метаболизма миокарда особое значение придается изменениям электролитного состава внутриклеточной и внеклеточной жидкости. Учитывая данный факт, наиболее существенным для миокарда являются перераспределение и дефицит калия. Поэтому диета, направленная на улучшение трофики миокарда, содержит повышенное по сравнению с обычным питанием количество калия. Это успешно достигается включением фруктов и овощей, отваров и настоев из них в рацион больных.
Другим важным компонентом для эффективного сокращения миокарда является кальций. Введение в пищу достаточного количества молочных продуктов, содержащих относительно большое содержание этого электролита, обычно достаточно для оптимального обеспечения миокарда кальцием. Дефицит некоторых микроэлементов, необходимых для нормального метаболизма сердечной мышцы, например, марганца и магния, возможный при инфаркте миокарда, вполне компенсируется использованием разнообразных продуктов как растительного, так и животного происхождения.
В целях снижения нагрузки на сердечно-сосудистую систему рекомендуется дробное питание, на 1–2 приема пищи больше, т. е. 5-6-разовое, и последний прием пищи разрешается не позднее, чем за 3 ч до сна. Кроме того, из диеты исключают продукты, оказывающие возбуждающее действие (крепкий чай, кофе, какао, шоколад, пряности и т. д.).
Лицам с избыточной массой тела необходимо нормализовать массу тела, поскольку это способствует нормализации нарушений липидного обмена, а также снижает физическую нагрузку на сердечную мышцу. Для таких больных рекомендуются разгрузочные дни. Можно рекомендовать следующие виды разгрузочных дней:
1) 500 г овсяной каши и 800 мл фруктового сока на день;
2) арбузный день (5 раз в день употреблять по 300 г спелого арбуза);
3) рисово-компотный день (5 стаканов компота, 100 г рисовой каши на день);
4) яблочный день (1,5–2 кг печеных или протертых яблок на день).
Диета № 10, разработанная институтом питания РАМН.
1. Жиры: рекомендуется ограничить прием всех жиров.
Ограниченный прием: масло и маргарин, содержащие полиненасыщенные жирные кислоты в большом количестве (в России – маргарин «Здоровье»). Масло: подсолнечное, кукурузное, шафрановое, соевое, оливковое, хлопковое.
Не рекомендуются: масло и жир, получаемые во время жаренья мяса и мясных продуктов, свиное сало, кокосовое масло. Маргарины без отметки о высоком содержании ненасыщенных жиров. Перетопленное или растительное масло неизвестного происхождения. Гидрогенизированные масла и маргарины.
2. Мясо.
Рекомендуются: нежирные сорта говядины, свинины, курицы, индейки, кролика в отварном или запеченном после отваривания виде, куском или рубленые, дичь (дикие утки, куропатки, зайчатина).
Ограниченный прием: постная говядина, бекон, ветчина, фарш из постной говядины, печень и почки.
Не рекомендуются: мясо с видимым жиром, грудинка и ребра баранины, свинина (мясо с области живота), бекон с прослойками жира, колбасы, сосиски, салями, паштет, яичница с мясом, утка, гусь, мясные пасты, кожа домашней птицы.
3. Молочные продукты.
Рекомендуются: снятое молоко, низко-жировые сыры (например, прессованный творог), сыр из снятого молока, из свернувшегося молока, кефир с низким содержанием жира.
Ограниченный прием: полуснятое молоко, сыры средней жирности (эдемский, камамбер). Плавленые, пастообразные сыры, 1–3 яйца в неделю, полужирные сыры, сметана только для заправки блюд.
Не рекомендуются: неснятое молоко, сгущенное и концентрированное молоко, сливки, взбитые сливки. Жирные сыры: чеддер, чеширский и т. п., сливочные сыры, жирный кефир.
4. Рыба.
Рекомендуются: вся «белая» рыба нежирных сортов в отварном или запеченном виде после отваривания: треска, ходдок, камбала. Жирная рыба: сельдь, макрель, сардины, тунец, лососевые (кета, горбуша, семга).
Ограниченный прием: рыба, приготовленная на пригодном масле. Моллюски. Морские ракообразные.
Не рекомендуется: икра рыбы.
5. Фрукты/овощи.
Рекомендуются: все свежие и замороженные, отварные и запеченные овощи, горох, фасоль, оливки. Картофель вареный, очищенный или «в мундире» (съедая кожуру, когда это возможно). Свежие фрукты, несладкие консервированные фрукты, грецкие орехи, каштан. Сухофрукты (чернослив, курага, изюм без косточек).
Ограниченный прием: жареный, тушеный картофель, приготовленный на пригодном масле, фрукты в сиропе, засахаренные фрукты, миндаль, лесной орех.
Не рекомендуются: виноградный сок, жареный, тушеный картофель (если он приготовлен на непригодном масле), картофельные чипсы, хрустящий картофель, шпинат, щавель, а также грибы, бобовые, редька и редис.
6. Злаки.
Рекомендуются: мука грубого помола (непросеянная), хлеб из нее, а также хлеб зерновой, с отрубями, обдирный, ржаной, немолотые (цельные) злаки, овсяная, пшеничная мука; овсяная каша на воде и молоке, пудинги, крупеники; неполированный рис и рисовая паста; макаронные запеканки, сухари, приготовленные в духовом шкафу, овсяное печенье, бездрожжевой хлеб.
Ограниченный прием: белая мука, белый хлеб, сладкие каши на завтрак, полированный (белый) рис и паста из него, обыкновенный полусладкий бисквит, бисквит, приготовленный на воде.
Не рекомендуются: пирожные, бисквиты с острым сыром, кондитерские изделия (печенье, пирожные), купленные в магазине.
7. Выпечка.
Рекомендуются: низкокалорийные пудинги: желе, щербет, пудинги из снятого молока, низкокалорийные приправы (пюре).
Ограниченный прием: пирожные, кондитерские изделия, бисквиты и приправы, приготовленные на пригодном масле или маргарине, домашние закуски на ненасыщенных жирах.
Не рекомендуются: пирожные, пудинги, бисквиты на насыщенных жирах, клецки, пудинги на нутряном жире, приправы на сливках и сливочном масле, все, купленные в магазине, пудинги и приправы, закуски, приготовленные на «кипящем» масле (жареные гарниры), молочное мороженое.
8. Напитки.
Рекомендуются: некрепкий чай и кофе, минеральная вода, несладкие напитки, фруктовые соки без сахара и разведенные, низкоалкогольное пиво.
Ограниченный прием: сладкие напитки, малосолодовые напитки, жидкий шоколад с низким содержанием жира (редко), пакетные супы, мясные супы, алкоголь.
Не рекомендуются: ирландский кофе (кофе со сливками и алкоголем), богатые жиром солодовые напитки, шоколад, сливочные супы.
9. Консервы, сладости.
Рекомендуются: «чистые» маринады, сладости без сахара: таблетки сахарина или жидкие сладости на аспартаме.
Ограниченный прием: сладкие маринады и приправы (из фруктов, перца), которые подают к холодному мясу (кэрри); мармелады, мед, сиропы, марципаны, арахисовое масло, лимонный творог; горячие сладости, пастила, мятные лепешки, сахар, сорбитол, глюкоза, фруктоза.
Не рекомендуются: шоколадные кремы, начинка для пирога на животных жирах, ириски, помадки, крем, полученный взбиванием масла и сахара, шоколад.
10. Остальное.
Рекомендуются: супы вегетарианские овощные, молочные, фруктовые, крупяные, щи, свекольник. Травы, специи, горчица, перец, уксус. Низкокалорийные приправы: лимон, йогурт, одно яйцо в день в виде белкового омлета.
Ограниченный прием: мясные и рыбные пасты, низкокалорийные сливки и майонез, бутылочные соусы, французские приправы, соевый соус.
Не рекомендуются: обычные салатные сливки, майонез, сливки или содержащие сливочный сыр приправы.
Запрещаются: крепкие мясные, рыбные, куриные и грибные бульоны, соления, копчености, бараний, свиной жир, сдобное тесто, соленая рыба, консервы, салями.
Пояснения к диетическим рекомендациям. «Рекомендуемые» продукты являются продуктами с низким количеством жиров и/или большим количеством волокон пектина.
Продукты, перечисленные в разделе «ограниченный прием», содержат полиненасыщенные жиры или небольшое количество насыщенных жиров. Если ваша диета будет содержать небольшое количество жиров, эти продукты допустимы ограничено. Например, «красное» мясо (ограниченный прием), т. е. не чаще трех раз в неделю, сыры средней жирности и рыбные пасты – 1 раз в неделю, или домашнее печенье, бисквиты, кондитерские изделия, приготовленные с использованием пригодных (содержащих полиненасыщенные жиры) маргарина или масла – дважды в неделю, или жареный картофель (печеный), приготовленный на соответствующем масле, один раз в две недели.
Продукты, перечисленные в разделе «не рекомендуются», содержат большое количество насыщенных жиров и должны быть исключены из питания настолько, насколько это возможно.
Больным, перенесшим инфаркт миокарда, у которых отсутствовал эффект от диеты № 10 и разгрузочных дней, при сопутствующей хронической недостаточности кровообращения 11Б и III стадий может быть назначена диета Карреля. Эта диета значительно разгружает обмен веществ, повышает диурез, уменьшает ацидоз. В диете резко ограничено содержание солей натрия и увеличено содержание калия. На 5-6-й день наступает лечебное действие диеты.
При наличии у больного, перенесшего инфаркт миокарда, артериальной гипертензии, недостаточности кровообращения может быть назначена калиевая диета. Данная диета обладает мочегонным действием, улучшает состояние миокарда, положительно влияет на натрикалиевый обмен, снижает артериальное давление. Калиевая диета содержит продукты, богатые калием и бедные натрием, и соотношение данных веществ должно быть не менее 8: 1 и не более 14: 1. В сутки содержание калия в диете должно составлять 5–7 г. В данную диету включены курага, изюм, орехи, печеный картофель, капуста, шиповник, апельсины, мандарины, персики, ячневая, овсяная, пшеничные крупы, крыжовник, чернослив, черная смородина, телятина, растительное масло, молоко нежирное и творог. Институтом лечебного питания РАМН разработано четыре варианта калиевой диеты, отличающиеся по содержанию калия и по химическому составу. Химический состав данной диеты неполноценный, учитывая это, ее назначают на 3–5 дней, начиная с первого рациона, по мере улучшения состояния больного переводят на последующие рационы. Продукты, богатые калием, вообще целесообразно включать в питание больных с хронической сердечной недостаточностью, особенно при лечении мочегонными средствами.
Вольных необходимо постоянно убеждать в важности соблюдения диеты, даже если отсутствует аппетит, следует съедать пищу.
Влагоприятное влияние на показатели липидного обмена оказывает питье минеральных вод.
Минеральные воды обладают желчегонным действием и способствуют снижению уровня холестерина в крови на 15% и тригли-церидов на 20% (Л. Е. Михно, К. Д. Вабов, 1995 г.). Рекомендуются преимущественно гидрокарбонатные натриевые, хлоридные, гидрокарбонатные сульфатные смешанного катионного состава минеральные воды. Наиболее широко применяются минеральные воды «Ессентуки» № 4, № 17, «Боржоми», «Смирновская», «Лужанская», «Арзни» и др.
Больным с клиническими проявлениями ИВС минеральные воды следует назначать в небольших количествах три раза в день (утром натощак, перед обедом и ужином) после предварительной их дегазации. Максимальную разовую дозу определяют исходя из массы тела больного: на 1 кг массы тела назначается 3,3 мл минеральной воды. При отсутствии сопутствующих заболеваний органов пищеварения минеральные воды больным ИВС назначают за 30 мин до еды, температура воды 36–37 °C. Продолжительность курса питьевого лечения колеблется от 3–4 до 5–6 недель. Повторный курс лечения минеральными водами на курорте рекомендуется больным ИВС через 9-12 месяцев. В домашних условиях лечение бутылочными минеральными водами можно проводить 2–3 раза в год с интервалами 4–6 месяцев. Для закрепления эффекта лечения минеральными водами на курорте целесообразно через 3–4 месяца провести амбулаторный курс лечения питьевыми минеральными водами.
Холестерин является структурным элементом всех клеточных мембран, предшественником синтеза желчных кислот и стероидных гормонов. Для этих нужд в организме человека синтезируется собственный эндогенный холестерин в достаточном количестве. При избыточном поступлении холестерина извне, т. е. с пищей, нарушается механизм обратной связи, и концентрация холестерина в крови значительно повышается.
В представленной диете предусмотрено ограничение содержания холестерина до 300–200 мг и даже 150 мг в сутки. Холестерин поступает в организм с продуктами животного происхождения. Вогаты холестерином следующие продукты: мозги, почки, печень, яичный желток, сливочное масло, свиной и бараний жир, жирное мясо и др. Рассчитано, что в среднем каждые 100 мг потребляемого холестерина увеличивают его содержание в крови на 10 мг/дл. Больному необходимо рассчитывать количество принятого холестерина с пищей в течение суток, для этого разработаны специальные таблицы. В некоторых случаях, чтобы снизить уровень холестерина, достаточно бывает просто ограничить пациента в потреблении жирных продуктов. Отказавшись от сала, колбасы, сливочного масла и заменив эти продукты рыбой и легкими маргаринами, больной может избежать повторного инфаркта миокарда.
Существует прямая взаимосвязь между потреблением с пищей морской рыбы, жира рыб, богатых полиненасыщенными жирными кислотами класса ω-3, и снижением заболеваемости и смертности от ишемической болезни сердца. Данный факт обусловлен нормализацией показателей липидного обмена, снижением агрегации тромбоцитов и вязкости крови при лечении жиром морских рыб. Жир морских рыб для лечения гиперлипидемий получают из тушек рыб, в отличие от рыбьего жира, получаемого из печени трески. Разработан новый пищевой продукт «Масло ихтеоновое пищевое» и в виде препарата – эйканол. Под влиянием пищевого ихтеонового масла снижается содержание общего холестерина, холестерина липопротеинов низкой плотности и очень низкой плотности, триглицеридов и повышается уровень холестерина антиате-рогенных липопротеинов высокой плотности. Применение ихтеоно-вого масла в течение года не вызывает изменений в функциональном состоянии печени. Через 4 месяца непрерывного лечения ихтео-новым маслом снижается частота приступов стенокардии, увеличивается продолжительность свободной ходьбы.
При лечении эйканолом возможны побочные явления в виде обострения хронических заболеваний желудочно-кишечного тракта (хронического гастрита, холецистита, язвенной болезни желудка, двенадцатиперстной кишки, хронического панкреатита). В этом случае лечение необходимо прекратить. При отсутствии эйканола и ихтеонового масла больной может получить эйкозопен-таеновую кислоту, употребляя в пищу рыбу и другие морепродукты. Содержание данного вещества в суточном рационе должно составлять 2–3 г. Содержание эйкозопентаеновой кислоты в граммах в 100 г продуктов наибольшее в ставриде – 1,44 г, в пасте «Океан» – 1,14 г, в сельди – 0,90 г, в сардинах – 0,86 г, в скумбрии от 0,7 до 1,26 г. При проведении диетотерапии целесообразно учитывать тип гиперлипопротеинемии.
Лекарственная реабилитация (коррекция дислипидемий, возможных осложнений)
Медикаментозное лечение дислипопротеинемий проводится в том случае, если строгая гиполипопротеинемическая диета, соблюдавшаяся не менее 6 месяцев, нормализация или снижение массы тела и физические нагрузки (тренировки) не приводят к адекватному снижению уровня липидов в крови. Для этого ориентируются на содержание в крови холестерина липопротеинов низкой плотности. Европейское общество по изучению атеросклероза рекомендует начинать одновременную медикаментозную терапию гиперхолестеринемии и диетотерапию при уровне холестерина в крови 250 мг/дл (6,5 ммоль/л). Задачей лечащих врачей является снижение уровня холестерина в плазме крови до 200 мг/дл (5,2 ммоль/л). Медикаментозная терапия дислипопротеинемий производится с учетом имеющегося у больного типа гиперлипиде-мии. Следует сказать, что нормальное или сниженное содержание в крови холестерина не является абсолютным показателем отсутствия активности атеросклеротического процесса в коронарных артериях. (См. табл. 1)
Таблица 1.
Нормальные значения показателей липидного спектра крови
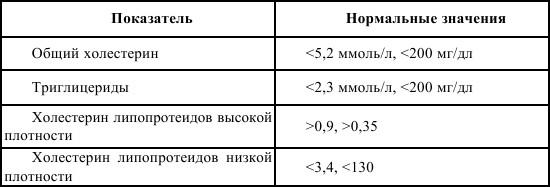
До начала медикаментозной терапии дислипопротеинемий необходимо определить содержание в крови холестерина, триглице-ридов и произвести фенотипирование гиперлипопротеинемий. Учитывая необходимость коррекции дислипидемий, лекарственная реабилитация после перенесенного инфаркта миокарда проводится гипохолестеринемическими препаратами из группы статинов – симвастатин (зокор), правастатин (липостат), флувастатин (лескол), а также никотиновой кислотой, гемфиброзилом, пробурколом. Ги-полипидемические (снижающие в крови уровень холестерина и триглицеридов) препараты в России включены в «Перечень жизненно необходимых и важнейших лекарственных средств». Классифицируется данная группа препаратов на пять групп:
1) ингибиторы 3-гидроксиметил-глютарил-коэнзим-А-редуктазы, или вастатины (или статины);
2) анионообменные смолы или секвестраты желчных кислот и средства, подавляющие абсорбцию холестерина в кишечнике;
3) никотиновая кислота и ее производные;
4) пробуркол;
5) фибраты, или производные фибровой кислоты.
Гиполипидемические средства также подразделяются с учетом их основного механизма действия:
1) препараты, препятствующие образованию атерогенных липо-протеинов;
2) препараты, тормозящие всасывание холестерина в кишечнике;
3) физиологические корректоры липидного обмена, содержащие эссенциальные фосфолипиды и ненасыщенные жирные кислоты, повышающие уровень липопротеинов высокой плотности.
Все перечисленные препараты назначаются пациентам с повышенным содержанием в крови холестерина и триглицеридов (соответственно гиперлипидемией и гипертириглицеридемией) на длительный период. Препараты позволяют снизить риск возникновения повторных сердечных приступов и других сердечно-сосудистых событий, а в случае их возникновения уменьшают риск смерти в первый год после развития инфаркта миокарда.
Механизм действия секвестратов желчных кислот заключается в следующем. Эти препараты, являясь анионообменными смолами, в кишечнике связываются с желчными кислотами, образуя с ними комплексы, и таким образом изолируют их (секвестрируют). Это приводит к затруднению обратного всасывания желчных кислот и увеличению выведения их с каловыми массами. Меньшее количество желчных кислот возвращается в печень, и возникает необходимость в образовании новых желчных кислот из холестерина. Соответственно увеличивается потребность в холестерине. Данная потребность обеспечивается увеличением синтеза холестерина в гепатоцитах и количества рецепторов, захватывающих из крови холестерин. Рецепторы и липопротеины низкой плотности, которые транспортируют холестерин, взаимодействуют друг с другом. Так происходит усиленное извлечение из крови холестерина, связанного с липопротеинами низкой плотности.
Секвестраты не оказывают серьезных побочных действий и не всасываются из просвета кишечника в кровь.
Препараты, замедляющие всасывание холестерина в кишечнике, уменьшают всасывание холестерина в кровь и, следовательно, снижают уровень холестерина в крови. К данным препаратам относятся диаспоний, или полиспонин, трибуспонин, гуарем. Полис-понин является сухим экстрактом из корней и корневищ диоско-реи ниппонской. В его состав входят водорастворимые стероидные сапонины, нарушающие всасывание холестерина из кишечника. Трибуспонин является препаратом, содержащим стероидные сапонины из травы якорцев стелющихся. Гипохолестеринемиче-ский эффект препарата выражен незначительно. Гуарем – препарат, являющийся естественной пищевой добавкой растительного происхождения. В его состав входят пищевые волокна, полученные из эндоспермы семян гиацинтовых бобов. Химической характеристикой данного вещества является его водорастворимость и то, что препарат является полисахаридом растительного происхождения.
Гуаровые волокна при контакте с водой образуют вязкое желе, которое не всасывается из желудочно-кишечного тракта. Под влиянием кишечных бактерий гуаровые волокна распадаются на короткие цепочки жирных кислот. Все это задерживает опорожнение желудка и время прохождения пищи по желудочно-кишечному тракту, а также желеобразная масса снижает процессы абсорбции.
Механизм гипохолестеринемического эффекта препарата гуа-рема объясняется следующим образом: гуарем снижает реабсорб-цию холестерина путем удаления его молекул с поверхности слизистой оболочки кишечника; препарат связывает желчные кислоты в кишечнике, уменьшая обратное поступление желчных кислот в печень, тем самым стимулируя их синтез в гепатоцитах; далее увеличивается количество рецепторов липопротеинов низкой плотности на поверхности гепатоцитов, это приводит к повышению захвата холестерина из плазмы крови; препарат снижает аппетит и количество потребляемой пищи, следовательно, приводит к снижению массы тела.
Выявлено и гипогликемическое действие гуарема, так как он уменьшает реабсорбцию углеводов в кишечнике.
В процессе клинических исследований препарата установлены также побочные эффекты гуарема: метеоризм, боли в области кишечника, тошнота, редко – рвота или жидкий стул.
Никотиновая кислота – водорастворимый витамин группы В, обладающий гиполипидемическим действием. Механизм ее действия заключается в подавлении мобилизации СЖК из жировой ткани, уменьшении образования в печени липопротеидов очень низкой плотности, снижении содержания в крови триглицеридов. Наряду с этим никотиновая кислота уменьшает образование и содержание в крови липопротеинов низкой плотности и холестерина. В отличие от других гиполипидемических средств никотиновая кислота снижает содержание в крови разновидности липопротеи-нов низкой плотности – липопротеина-а. Данный препарат активирует систему фибринолиза и увеличивает размер липопротеинов низкой плотности, что значительно затрудняет инфильтрирование их в интиму артерий. Никотиновая кислота повышает уровень холестерина липопротеинов высокой плотности (атиатерогенных липопротеинов), в том числе и при нормолипидемии; установлено, что этот эффект выражен больше, чем у всех других гиполи-пидемических средств.
Применение никотиновой кислоты с секвестрантами желчных кислот способствует стабилизации и регрессии стенозов коронарных артерий. При терапии никотиновой кислотой могут наблюдаться побочные явления со стороны функции печени, желудка, у большинства больных в начале применения может наблюдаться гиперемия кожи, возможно развитие гипергликемии.
Разработана новая пролонгированная форма никотиновой кислоты – эндурацин. Этот препарат хорошо всасывается из желудочно-кишечного тракта и почти не дает побочных эффектов. Эндурацин обладает гиполипидемическим и антиагрегатным действием, а также расширяет коронарные артерии.
Пробуркол является эффективным гипохолестеринемическим средством, снижающим содержание в крови холестерина, но на уровень триглицеридов пробуркол практически не влияет. Пробур-кол активирует нерецепторный путь удаления из крови липопро-теинов низкой плотности соответственно холестерина; увеличивает содержание в крови протеина, переносящего эфиры холестерина, благодаря чему активируется «обратный» транспорт холестерина, т. е. перенос его из клеток органов и тканей в печень с последующим удалением его из организма. Выявлено его антиоксидантное действие, препарат уменьшает способность липопротеинов низкой плотности проникать в субэндотелиальный слой, окисляться.
Фибраты – производные фибровой кислоты. К ним относятся гиполипидемические средства, оказывающие преимущественно гипотриглицеридемическое действие. Данная группа препаратов представлена гемфиброзилом, фенофибратом, безафибратом, кло-фибратом. В исследованиях установлено, что данные лекарственные вещества снижают уровень холестерина липопротеинов низкой плотности на 5-15%.
Гемфиброзил (лопид, гевилон) – фибрат II поколения, не только снижающий содержание в крови триглицеридов и в меньшей степени холестерина, но также повышающий уровень в крови холестерина ЛПВП. К сожалению, в Российскую Федерацию оригинальный гемфиброзил не поставляется, есть только его генери-ческая копия – изолипан.
Показания к назначению гемфиброзила:
1) основное показание – уменьшение риска развития ИБС у лиц с ПБ типом гиперлипопротеинемии без признаков заболеваний коронарных артерий в настоящем или прошлом с триадой липидных нарушений: низкий холестерин, липопротеины низкой плотности, повышенный холестерин ЛПНП, высокий уровень триглицеридов в крови;
2) резкое увеличение содержания в крови триглицеридов (до 11,3 ммоль/л и более);
3) гиперлипопротеинемия III типа с увеличением содержания в крови липопротеинов промежуточной плотности, при этом в крови повышено содержание холестерина и триглицеридов;
4) гипертриглицеридемия и снижение содержания в крови холестерина ЛПВП у больных инсулиннезависимым сахарным диабетом.
Гемфиброзил принимают за 30 мин до завтрака и ужина по 450–600 мг (суточная доза 900-1200 мг).
Побочные действия гемфиброзила проявляются поражением мышц (повышенная чувствительность, боли, слабость в мышцах, повышение креатинкиназы в крови), в этом случае лечение следует прекратить; способностью усиливать камнеобразование в желчных путях; диспептическими расстройствами (тошнота, иногда рвота), болями в животе; ухудшением функции печени, при печеночной патологии гемфиброзил не применяется. В редких случаях возможно развитие лейкопении, тромбоцитопении, анемии.
Безафибрат (безалип) – применяется значительно реже, чем гемфиброзил, так как уступает последнему по степени снижения триглицеридов в крови. Имеет те же показания, что и фенофиб-рат. Рекомендуемая суточная доза – 200 мг 3 раза в день, а при приеме пролонгированной формы – 400 мг один раз в день. У больных с любым типом гиперлипопротеидемии препарат повышает уровень холестерина ЛПВП, что отмечается как у больных с первичной гиперлипидемией, так и с вторичной, обусловленной сахарным диабетом или заболеванием почек. При длительном применении безафибрата (от 2 до 4 лет) отмечаются стабильные результаты, развития толерантности не наблюдается. По гиполи-пидемической эффективности препарат не уступает клофибрату, фенофибрату, а степень повышения уровня холестерина липопро-теинов высокой плотности выше. Хорошо всасывается в желудочно-кишечном тракте. Побочные эффекты: в основном это желудочно-кишечные расстройства, реже – кожные реакции и др. Случаев гепатотоксичности за период клинического использования препарата не зарегистрировано, нет и доказательств более частого образования желчных камней у пациентов, длительно лечащихся безафибратом.
Фенофибрат (липантил) – назначается по 100 мг три раза в день. Имеется пролонгированная форма препарата, принимаемая один раз в день. Установлено, что лечение фенофибратом позволяет добиться снижения содержания холестерина на 13%. Препарат снижает также содержание триглицеридов в крови. Побочные действия те же, что у гемфиброзила. Положительная особенность его по сравнению с другими фибратами – снижение уровня мочевой кислоты на 10–28%, что позволяет отдавать предпочтение фенофибрату при лечении больных с сочетанием гиперлипиде-мии и гиперурикемии. Кроме того, этот препарат наряду с ципро-фибратом наиболее эффективно снижает уровень триглицеридов в липопротеидах очень низкой плотности. Используется при всех типах гиперлипидемии за исключением I типа. Побочные эффекты наблюдаются нечасто (от 2% до 15% случаев). Это желудочно-кишечные расстройства (запоры или диарея), редко – кожные проявления (зуд, покраснение, сыпь), которые быстро самостоятельно проходят после отмены препарата. В единичных случаях отмечаются миалгия, сопровождавшаяся повышением уровня кре-атинфосфокиназы, импотенция, общая слабость, головная боль, головокружение, бессонница. В некоторых случаях повышается уровень трансаминаз в крови, в то время как содержание у-глута-милтранспептидазы и щелочной фосфатазы часто снижается. Есть данные о возрастающей литогенности желчи по сравнению с тем, что наблюдалось до лечения фенофибратом. До настоящего времени нет данных, свидетельствующих об увеличении частоты образования желчных камней на фоне терапии этим препаратом.
Липантил 200М – микроионизированная капсульная форма фенофибрата, обладающая продленным действием. Препарат назначается один раз в сутки в дозе 200 мг во время вечернего приема пищи. Лечение может проводиться в течение нескольких месяцев. Препарат показан при 11А, 11В, III и IV типах гиперлипопротеине-мии, особенно при выраженной гипертриглицеридемии, высоком уровне в крови холестерина ЛПНП. Клофибрат (мисклерон) – первый препарат из группы фибратов. Клофибрат активирует ли-попротеинлипазу и ускоряет метаболизм ЛПОНП и ЛППП, снижая их содержание в плазме крови. Влияние на уровень ЛПНП непостоянно. В настоящее время клофибрат практически не используется в связи с увеличением частоты образования камней в желчном пузыре, а также вследствие повышения смертности от внесердечных причин.
В связи с выраженным побочным действием применяют кло-фибрат относительно редко. В основном препарат эффективен при III типе гиперлипопротеинемии. Назначается внутрь.
Основными побочными эффектами являются тошнота, рвота, диарея, холелитиаз, мышечные боли, сердечные аритмии, кожные высыпания, импотенция.
Ципрофибрат – фибрат III поколения, применяется в суточной дозе 100–200 мг. Обладает теми же побочными действиями, что и гемфиброзил.
Таким образом, фибраты (производные фибровой кислоты) применяются при лечении очень высоких уровней триглицеридов в крови (IV тип гиперлипопротеинемии), для лечения больных семейной гиперлипопротеинемией III типа, при комбинированной гиперлипопротеинемии и у больных сахарным диабетом с повышенным уровнем триглицеридов в крови («Второй доклад экспертов Национальной образовательной программы по холестерину США», 1993 г.). Однако при лечении фибратами IV типа гипер-липопротеинемии возможно повышение содержания ХС ЛПНП в крови. В этом случае необходимо лечение фибратами и секвест-рантами желчных кислот.
Ингибиторы 3-гидрокси-3-метилглутарил-коэнзима-А-редукта-зы (статины). Ингибиторы 3-гидрокси-глютарил-коэнзим-А-редук-тазы (ГМК-КоА-редуктазы), или вастатины (статины).
Статины являются наиболее активными гипохолестеринеми-ческими средствами. Механизм действия:
1) установлено, что в процессе образования холестерина в клетке участвует фермент ГМГ-КоА-редуктаза. Статины блокируют
активность этого фермента, что приводит к уменьшению образования холестерина;
2) снижение синтеза холестерина в гепатоцитах сопровождается увеличением синтеза большого количества рецепторов для ли-попротеинов низкой плотности, и происходит повышенное извлечение из крови и дальнейшее снижение уровня липопротеи-нов низкой плотности;
3) увеличение числа рецепторов липопротеина низкой плотности способствует снижению в крови уровня и их предшественников – ЛПОНП, что также способствует снижению и ЛПНП, и общего холестерина.
Ловастатин (мевакор) – это неактивный лактон, выделенный из гриба АврегдШш 1еггеи8. В печени это лекарственное вещество превращается в активное соединение, которое захватывается ге-патоцитами, и в них осуществляет свое ингибирующее влияние на фермент ГМГ-КоА-редуктазу, в результате чего снижается синтез холестерина и ЛПНП.
В начале лечения препарат назначается по 20 мг один раз в сутки во время ужина. Однократный прием вечером более эффективен по сравнению с утренним приемом. Это объясняется тем, что холестерин синтезируется главным образом в ночные часы. Установлено, что снижение общего холестерина крови достигает 30%, увеличивается уровень холестерина ЛПВП, уменьшается содержание в крови триглицеридов. Лечение ловастатином можно продолжать длительно (несколько месяцев и даже лет), так как препарат является достаточно безопасным.
Симвастатин (зокор) – как и ловастатин, получен из грибов, является неактивным соединением, в печени превращается в активное вещество, ингибирующее ГМГ-КоА-редуктазу. Симваста-тин применяется в суточной дозе 20–40 мг.
Правастатин – является активной формой, оказывает антили-пидемическое действие без предварительного метаболизма в печени. Является производным грибковых метаболитов. Суточная доза правастатина составляет 20–40 мг. Под влиянием лечения правастатином количество ХС ЛПНП снижается, уровень ХС ЛПВП повышается. Установлено замедление прогрессирования коронарного атеросклероза, положительное влияние на клиническое течение ишемической болезни сердца, инфаркта миокарда и уменьшение случаев смертности как от ИБС, так и «несердечной» смерти. Переносимость препарата хорошая. Лечение может продолжаться несколько месяцев и даже лет.
Флувастатин (лескол) – новый, полностью синтетический ингибитор ГМГ-КоА-редуктазы. В отличие от ловастатина, симваста-тина и правастатина, этот препарат не является производным грибковых метаболитов, основа его молекулы – индольное кольцо. Данный препарат – исходно активный препарат в отличие от других статинов. Флувастатин назначается в вечернее время в суточной дозе 20–40 мг; переносимость и эффективность его не зависят от времени приема пищи. Гиполипидемический эффект флувастатина развивается уже в течение первой недели, достигает максимума через 3–4 недели и сохраняется на достигнутом уровне при продолжении лечения.
Аторвастатин является новым синтетическим ингибитором ГМГ-КоА-редуктазы с выраженным гипохолестеринемическим эффектом, а также препарат значительно снижает уровень триглице-ридов. Применяется при гиперлипопротеинемии НА, ПБ, IV типов в дозе 5-10 мг/сут.
Статины (вастатины) являются достаточно безопасными, хорошо переносимыми гиполипидемическими средствами. Однако иногда могут возникать побочные явления.
Влияют на печень. Статины действуют избирательно в клетках печени. Поэтому примерно у 1% больных возможно повышение содержания в крови АлАТ, обычно при применении больших доз препаратов. Вероятность поражения печени возрастает при сочетанном применении статинов и фибратов. Указанные изменения быстро проходят после прекращения приема препаратов. Влияют на мышечную ткань. У некоторых больных может наблюдаться боль в мышцах, мышечная слабость, повышение содержания в крови креатинфосфокиназы. Опасность поражения мышц возрастает при одновременном использовании статинов и фибра-тов. Желудочно-кишечные расстройства: тошнота, снижение аппетита, запоры, метеоризм. Могут наблюдаться расстройства сна, преимущественно при применении ловастатина и симвастина. При лечении правастатином возможна головная боль.
Не выявлено отрицательного воздействия статинов на углеводный и пуриновый обмен, что позволяет активно применять эти средства при лечении гиперлипопротеинемии у больных сахарным диабетом, ожирением, подагрой, бессимптомной гиперури-кемией.
Главной характеристикой действия статинов является антиа-терогенный эффект. Статины обладают множеством дополнительных свойств, не связанных с воздействием на уровень липидов.
Вольшая их часть улучшает течение атеросклеротических заболеваний, участвует в быстром (в течение месяца) снижении смертности. Поэтому статины рекомендуются независимо от уровня липидемии всем больным с острым инфарктом миокарда. В основном эти свойства связаны с восстановлением нарушенной при атеросклерозе функции эндотелия коронарных артерий. Дополнительные эффекты в той или иной мере присущи всем статинам и, в меньшей степени, другим липидкорригирующим средствам.
Гиполипидемические средства необходимо назначать с учетом типа гиперлипидемии, а также уровня в крови общего холестерина и триглицеридов.
В некоторых случаях применяется комбинированная медикаментозная гиполипидемическая терапия. Комбинированная терапия проводится при ярко выраженной гиперхолестеринемии, в целях снижения уровня холестерина липопротеинов низкой плотности часто используют диетотерапию и два препарата, рекомендуют сочетание секвестрантов желчных кислот с никотиновой кислотой или ловастатином. При одновременном повышении уровня холестерина липопротеинов низкой плотности и триглицеридов рекомендуется сочетание секвестрантов желчных кислот с никотиновой кислотой или гемфиброзилом.
К гиполипидемическим средствам относятся также бензафла-вин, эссенциале и липостабил.
Вензафлавин – производное рибофлавина-2, 3, 4, 5 – тетра-бензоил-5-ацетил-1,5-дигидрорибофлавина. Препарат повышает содержание в печени флавинов и восстанавливает энергетический обмен в митохондриях печени. Кроме того, бензафлавин понижает содержание в крови глюкозы, холестерина, триглицеридов, ли-попротеинов. Начало гиполипидемического действия препарата отмечается уже на 2-4-й день лечения. Вензафлавин назначается внутрь по 0,04-0,06 г 1–2 раза в день. Переносимость препарата хорошая, побочных эффектов нет, лечение продолжается несколько месяцев.
Эссенциале является комплексным препаратом, содержащим эссенциальные фосфолипиды, ненасыщенные жирные кислоты, витамины В12, никотинамид, натрия пантотенат. Установлено, что препарат усиливает катаболизм холестерина. Наиболее эффективен при ИЛ и ИВ типах гиперлипопротеинемии. Назначают по две капсулы три раза в день в течение 2–3 месяцев 3–4 раза в год. Эссенциальные фосфолипиды улучшают способность липопротеинов высокой плотности извлекать из артерий и транспортировать холестерин, т. е. эссенциале повышает антиатероген-ные холестерин-акцепторные и холестерин-транспортные свойства липопротеинов высокой плотности.
Липостабил – это препарат, близкий по механизму действия к эссенциале. Применяется для лечения гиперхолестеринемии и ги-пертриглицеридемии, но чаще при НА и ПБ типах гиперлипо-протеинемии. Применяется внутрь в капсулах – 1–2 капсулы три раза в день в течение трех месяцев.
Целесообразна в комплексном лечении больных атеросклерозом поливитаминотерапия, так как она способствует катаболизму атерогенных липопротеинов и улучшает метаболические процессы в миокарде, печени, головном мозге. Основными предпосылками для поливитаминотерапии при инфаркте миокарда являются следующие:
1) повышенная потребность в витаминах у больных атеросклерозом, ИБС;
2) снижение активности витаминсодержащих ферментов, что ведет к нарушению аэробного, анаэробного гликолиза, цикла Креб-са с накоплением в организме пировиноградной и молочной кислот;
3) нарушение липидного обмена и белкового обмена, усиление перекисного окисления липидов;
4) снижение сократительной способности миокарда у больных ИБС.
Поливитаминотерапия больных инфарктом миокарда проводится курсами по 1–2 месяца, которые повторяют 3–4 раза в год, особенно в сезоны дефицита витаминов в рационе больного. Применяются препараты «Ундевит», «Декамевит», «Олиговит», «Фор-тевит» и др.
Витаминотерапия больных атеросклерозом должна проводиться с учетом межвитаминных взаимоотношений. Установлено, что моновитаминотерапия может проводиться только витаминами, не обладающими антагонистическим действием друг на друга. Такими витаминами являются В, Н (биотин), С, пантотеновая кислота.
Витаминотерапия при атеросклерозе должна применяться в виде сбалансированных поливитаминных комплексов, которые способствуют ассимиляции витаминов, обеспеченность которыми в организме снижена, нивелированию конкурентных отношений между витаминами и нормализации метаболических процессов.
Максимальное терапевтическое действие витаминных комплексов достигается после 3-4-недельного курса лечения и сохраняется в течение 2–4 недель. Рекомендуется через 1,5–2 месяца проводить повторные курсы витаминотерапии. Фитотерапия.
Препараты лекарственных растений назначают в реабилитационном периоде после перенесенного инфаркта миокарда для предупреждения развития атеросклероза. С целью предупреждения хорошо себя зарекомендовали профилактические поливитаминные и регулирующие обмен веществ чаи. Фитотерапия проводится обычно в течение двух месяцев, затем делают перерыв на 1,5–2 месяца, после чего курсы снова неоднократно повторяют. Настои и чаи могут назначаться для предупреждения развития атеросклероза, с гипохолестеринемической целью, регулирования обменных процессов в организме, для снижения артериального давления и т. д.
Предупреждение развития атеросклероза
1. Смородина черная (листья) – 1 часть.
Малина обыкновенная (листья) – 1 часть.
Ежевика сизая (листья) – 1 часть.
Шиповник коричный (плоды) -1 часть.
Земляника лесная (листья) – 1 часть.
Приготовление: 1 ст. л. смеси заваривают 2 стаканами кипятка, кипятят 10 мин, настаивают 2 ч в закрытой посуде, процеживают. Пьют по 1 стакану 2 раза в день. Поливитаминные чаи при систематическом употреблении стимулируют обмен веществ, кроветворение и повышают активность защитных систем организма.
Регулирование обменных процессов в организме
2. Ежевика сизая (листья) – 2 части.
Земляника лесная (листья) – 3 части.
Шиповник коричный (плоды и листья) – 3 части.
Земляника лесная (листья) – 3 части.
Ежевика сизая (листья) – 2 части.
Тимьян ползучий (чабрец) (трава) – 1 часть. Костяника лесная (листья) – 2 части.
Приготовление: аналогично вышеприведенным примерам. Шиповник, содержащийся в сборах, перед заваркой следует измельчить. В чай добавляют по вкусу мед или сахар.
При повышенном содержании холестерина в крови
3. Шиповник коричный (плоды) – 2 части.
Сушеница болотная (трава) – 1 часть.
Береза повислая (листья) – 1 часть.
Мята перечная (листья) – 1 часть.
Морковь посевная (плоды) – 1 часть. Элеутерококк колючий (корень) – 1 часть. Кассия остролистная (плоды и листья) – 1 часть. Почечный чай (трава) – 1 часть. Лопух большой (корень) – 1 часть.
Принимают в виде настоя по 1/2 стакана 3 раза в день после еды. 4. Арника горная (цветки) – 1 часть. Тысячелистник обыкновенный (трава) – 4 части. Зверобой продырявленный (трава) – 4 части. Принимают в виде настоя. Стакан выпивают глотками в течение дня.
При повышенном кровяном давлении
Воярышник кроваво-красный (цветки) – 2 части.
Хвощ полевой (трава) – 1 часть.
Омела белая (трава) – 1 часть.
Варвинок малый (трава) – 1 часть.
Тысячелистник обыкновенный (трава) – 1 часть.
Принимают в виде настоя по 1/2 стакана 3 раза в день после еды.
При избыточной массе тела
Арника горная (цветки) – 1 часть.
Тысячелистник обыкновенный (трава) – 1 часть.
Зверобой продырявленный (трава) – 1 часть.
Крушина ольховидная (кора) – 1 часть.
Петрушка кудрявая (плоды) – 1 часть.
Принимают в виде настоя по 1/2 стакана 3 раза в день после еды.
Нарушения ритма сердца и проводимости являются наиболее частыми осложнениями инфаркта миокарда. По данным Е. И. Чазова (1974 г.), они наблюдаются при электрокардиографическом мониторном наблюдении у больных с крупноочаговым инфарктом миокарда в 87-100% случаев, с мелкоочаговым – в 71%.
По данным Э. Гольдбергер и М. Вит (1979 г.) сердечные аритмии, вызванные инфарктом миокарда, в зависимости от прогноза классифицируются на три группы:
1) существенно не влияющие на прогноз и, следовательно, не требующие срочных лечебных мероприятий, т. е. прогностически индифферентные;
2) существенно отягощающие состояние больного, поэтому требующие экстренного антиаритмического лечения (прогностически серьезные);
3) представляющие угрозу для жизни больного, следовательно, требующие немедленной антиаритмической терапии, а в ряде случаев реанимационных мероприятий.
Если частота сокращений желудочков составляет 50–60 в минуту, нет артериальной гипотензии и желудочковых аритмий, синусовая брадикардия не требует лечения.
При необходимости терапии синусовой брадикардии больному назначается внутривенное введение атропина сульфата. Обычно продолжительность лечения атропином составляет одни сутки.
При отсутствии эффекта от лечения атропином или при наличии противопоказаний для его применения (глаукома, парез мочевого пузыря, гипертрофия предстательной железы) применяются стимуляторы адренергических рецепторов – изопротеренол (изадрин, изупрел), алупент. Установлено, что лечение данными препаратами противопоказано при сопутствующей желудочковой экстрасистолии, так как они повышают возбудимость миокарда.
При синусовой брадикардии в сочетании с артериальной гипо-тензией целесообразно использовать положение больного с приподнятыми на 45° нижними конечностями, что увеличивает венозный возврат и может повысить ЧСС и уровень АД.
Предсердная экстрасистолия не требует специального лечения, но иногда может быть предвестником мерцательной аритмии. Лечение предсердной экстрасистолии следует проводить, если наблюдается более 6 экстрасистол в минуту или если регистрируется предсердная экстрасистолия в виде бигеминии или тригеминии, или если экстрасистолия сопровождается клиническим ухудшением состояния больного.
Желудочковая экстрасистолия является наиболее частой формой аритмий у больных инфарктом миокарда. Желудочковая экстра-систолия иногда предшествует фибрилляции желудочков.
Критериями для начала лечения желудочковой экстрасисто-лии при инфаркте миокарда являются:
1) появление желудочковых экстрасистол в «ранимый» период сердечного цикла (т. е. на восходящем колене и вершине зубца Т – ранние экстрасистолы типа «К на Т»);
2) частота желудочковой экстрасистолии более 5 в минуту;
3) эпизоды парных или групповых экстрасистолий;
4) политопная (полиморфная) желудочковая экстрасистолия;
5) возобновление экстрасистолии после уже перенесенной фибрилляции желудочков или желудочковой пароксизмальной тахикардии.
Препаратом выбора при желудочковой экстрасистолии на фоне инфаркта миокарда считается лидокаин. Противопоказания к введению лидокаина: слабость синусового узла; атриовентрикуляр-ная блокада II–III ст.; резко выраженная брадикардия; кардио-генный шок; тяжелые нарушения функции печени.
Новокаинамид (прокаинамид) применяется при повышенной чувствительности к лидокаину или в случае недостаточной его эффективности. Новокаинамид применяется для купирования желудочковой экстрасистолии при инфаркте миокарда и является альтернативой лидокаину.
Целесообразно при лечении новокаинамидом проводить мониторинг его концентрации в крови. Эффективная терапевтическая концентрация новокаинамида в плазме крови, при которой не возникает серьезных гемодинамических нарушений, составляет 4–8 мкг/мл. Период полувыведения препарата 3–5 ч. Не рекомендуется лечение новокаинамидом при выявлении артериальной гипотензии и замедлении внутрижелудочковой проводимости.
Для лечения желудочковой экстрасистолии у больных инфарктом миокарда при неэффективности лидокаина и новокаинамида используется бретилия тозилат (орнид). Препарат резко повышает порог фибрилляции желудочков и оказывает таким образом анти-фибрилляторное действие. Лекарственное средство хорошо переносится, не угнетает сократительную способность миокарда. Самый серьезный побочный эффект при введении бретилия – артериальная гипотензия. Во время инфузии препарата больной должен находиться в горизонтальном положении.
Эсмолол – в-адреноблокатор – с успехом применяется при инфаркте миокарда (когда экстрасистолия обусловлена избыточной симпатической стимуляцией) и при гликозидной интоксикации. Следует помнить об основных побочных действиях в-адре-ноблокаторов: снижение сократимости миокарда; брадикардия; замедление атриовентрикулярной проводимости; замаскированная гипогликемия; артериальная гипотензия; бронхоспазм, мышечная слабость.
Мексилетин – структурный аналог лидокаина, препарат из I класса антиаритмических средств, блокирует быстрые натриевые каналы, уменьшает максимальную скорость потенциала действия. Мекселитин не вызывает серьезных гемодинамических нарушений при инфаркте миокарда, однако возможны следующие побочные действия: замедление атриовентрикулярной проводимости, диспептические расстройства при приеме внутрь, брадикардия.
Кордарон может применяться для купирования желудочковой экстрасистолии при инфаркте миокарда.
Пропафенон (ритмонорм) сочетает свойства антиаритмических препаратов 1С класса, так как блокирует быстрые натриевые каналы, и в-адреноблокаторов, так как является некардиоселективным в-адреноблокатором. К побочным действиям ритмонорма относятся аллергические проявления (покраснение и зуд кожи, экзантемы, крапивница), нарушения сна, головная боль, снижение функции синусового узла, развитие брадикардии, замедление атриовентрикулярной проводимости, возможно усиление недостаточности кровообращения, лейкопения и тромбоцитопения (редко).
Пароксизмальная суправентрикулярная тахикардия наблюдается у 2–5% больных инфарктом миокарда. При этом увеличивается потребность миокарда в кислороде, что может вызвать значительное ухудшение состояния больных. При удовлетворительном состоянии больного, отсутствии гемодинамических нарушений можно вначале использовать рефлекторные методы купирования. Они основаны на раздражении блуждающего нерва: пробу Чермака– Геринга (массаж области каротидного синуса), пробу Ашнера-Да-нини (надавливание на глазные яблоки), пробу Вальсальвы (выдох при закрытой голосовой щели, или проба с натуживанием). Эти пробы оказываются эффективными в 50% случаев пароксизмальной суправентрикулярной тахикардии (прежде всего при предсердной форме). При отсутствии эффекта от рефлекторных проб средством выбора считается внутривенное введение натрия аденозинтрифосфа-та. Препаратом второй очереди является финоптин, или изоптин. К лечению этим препаратом прибегают при отсутствии АТФ натрия или его неэффективности.
Мерцательная аритмия имеет большое прогностическое значение в связи с тем, что частое сокращение желудочков при тахи-систолической форме может вызвать нарушение гемодинамики. При терапии этого осложнения инфаркта миокарда в первую очередь необходимо добиться урежения ЧСС (если это тахисистоли-ческая форма мерцательной аритмии). С этой целью назначается дигоксин внутривенно. Лечение данным препаратом в ряде случаев позволяет не только добиться урежения ЧСС, но и восстановить синусовый ритм. Противопоказаниями к назначению антагонистов кальция изоптина и дилтиазема являются выраженная недостаточность кровообращения, нарушение атриовентрикуляр-ной проводимости, синдром слабости синусового узла, артериальная гипотензия. Если мерцательная аритмия существовала у больного длительное время до развития инфаркта миокарда, то ограничиваются лишь нормализацией числа сокращений желудочков, восстановление синусового ритма не производится. Для профилактики приступов мерцательной аритмии рекомендуется корда-рон в сочетании с анаприлином или финоптином.
Трепетание предсердий наблюдается у 1–6% больных инфарктом миокарда. Прогностическое значение этого вида аритмии неблагоприятное, так как обычно число сокращений желудочков превышает 150–160 в минуту и сопровождается снижением минутного объема, что приводит к недостаточности кровообращения.
При лечении трепетания предсердий у больного инфарктом миокарда методом выбора является электрическая дефибрилляция с использованием разряда в 2500–3000 В. При отсутствии эффекта от первого разряда производится второй. Нередко после второго разряда трепетание предсердий переходит в мерцание, для купирования которого рекомендуется произвести третий разряд.
Медикаментозная терапия трепетания предсердий допустима только в случае, если нет угрожающих симптомов сердечной недостаточности или невозможно проведение электроимпульсной терапии. Активно используется лечение дигоксином. Сердечные гли-козиды замедляют ритм желудочковых сокращений и переводят трепетание предсердий в мерцание. После этого дигоксин необходимо отменить. Часто после его отмены мерцание предсердий самопроизвольно исчезает и синусовый ритм восстанавливается. У некоторых больных происходит восстановление синусового ритма без перехода трепетания предсердий в мерцание.
Необходимо помнить, что после струйного внутривенного введения сердечных гликозидов запрещено прибегать к электроимпульсной терапии. При продолжающемся приступе трепетания предсердий на фоне приема сердечных гликозидов необходимо проводить стимуляцию предсердий из правого предсердия или пищевода.
При отсутствии такой возможности необходимо ввести внутривенно медленно (в течение 5 мин) 10 мл 10%-ного раствора но-вокаинамида с 10 мл изотонического раствора натрия хлорида под тщательным контролем АД. Выявлена меньшая опасность внутривенного капельного введения 10 мл 10%-ного раствора новокаин-амида в 100 мл изотонического раствора натрия хлорида со скоростью 40–45 капель в минуту. Установлено, что после введения новокаинамида допустимо проведение электроимпульсной терапии (Н. А. Сысоева, 1993 г.). В ряде случаев удается купировать трепетание предсердий внутривенным введением новокаинамида, кордарона, обзидана. После восстановления синусового ритма назначается профилактическая терапия аналогично таковой при мерцании предсердий.
Лечение пароксизмальной желудочковой тахикардии Пароксизмальная желудочковая тахикардия встречается у 10% больных инфарктом миокарда.
Согласно В. Н. Захарову (1990 г.), с точки зрения терапевтической тактики, выделяют три типа пароксизмальной желудочковой тахикардии.
1-й тип – кратковременная (залп из 3–6 желудочковых экстрасистол).
2-й тип – длительная, без нарушения гемодинамики.
3-й тип – длительная, с признаками острой левожелудочковой недостаточности или аритмической формы кардиогенного шока.
Медикаментозное купирование пароксизмальной желудочковой тахикардии производится при первом и втором типах. Н. М. Шевченко и А. А. Гросу (1992 г.) рекомендуют купировать пароксиз-мальную желудочковую тахикардию следующим образом.
1. Вводится внутривенно струйно в течение 1 мин 100 мг ли-докаина (5 мл 2%-ного раствора). Купирующий эффект лидокаи-на не превышает 30%, однако имеются следующие преимущества лидокаина: быстрота и кратковременность действия, невысокая токсичность.
2. При отсутствии эффекта от лидокаина вводится внутривенно медленно новокаинамид в дозе 1 г (10 мл 10%-ного раствора в 10 мл изотонического раствора натрия хлорида) в течение 5–6 мин под тщательным контролем артериального давления. Менее опасно внутривенное капельное введение 10 мл новокаинамида в 100 мл изотонического раствора натрия хлорида в течение 30–40 мин. В процессе введения новокаинамида возможно дополнительное введение болюсом лидокаина (2,5 мл 2%-ного раствора), так как при сочетании лидокаина и новокаинамида антиаритмический эффект усиливается.
Вместо новокаинамида вторым препаратом (т. е. препаратом второй очереди) может быть:
1) дизопирамид, или ритмилен, назначаются внутривенно в дозе 150 мг за 3 мин;
2) этмозин применяется внутривенно в дозе 150 мг за 3 мин (6 мл 2,5%-ного раствора);
3) гилуритмал, или аймалин – в дозе 50 мг за 3 мин (2 мл 2,5%-ного раствора).
Купирующий эффект препаратов новокаинамида, дизопира-мида, этмозина, гилуритмала приблизительно одинаков.
3. При отсутствии желаемого клинического эффекта от препаратов первого и второго рядов следует применить кордарон в дозе 150–300 мг (3–6 мл 5%-ного раствора в 20 мл изотонического раствора натрия хлорида внутривенно медленно в течение 5– 10 мин).
4. В некоторых случаях при отсутствии эффекта от применения вышеназванных препаратов можно вводить обзидан.
Обзидан вводится внутривенно медленно в количестве 5-10 мг со скоростью 1 мг/мин (т. е. 5-10 мл 0,1%-ного раствора в 10 мл изотонического раствора натрия хлорида со скоростью 2 мл/мин). Может быть эффективным внутривенное введение ритмонорма в дозе 20 мл (70 мг) в течение 5–6 мин.
После купирования пароксизмальной желудочковой тахикардии с профилактической целью можно назначить внутрь новока-инамид в суточной дозе 3 г, кордарон – по 0,2 г 1 раз в день 5 дней в неделю, аймалин – 300 мг в сутки и др.
Лечение при нарушениях атриовентрикулярной проводимости
Атриовентрикулярная блокада I ст. (замедление атриовентри-кулярной проводимости) возникает у 4-14% больных инфарктом миокарда преимущественно задней стенки левого желудочка и обусловлена ишемией атриовентрикулярного соединения. Обычно атриовентрикулярная блокада I ст. имеет преходящий характер и благоприятный прогноз, а также не требует специального лечения. Следует учесть, что иногда замедление атриовентрикуляр-ной проводимости может быть обусловлено лечением а-адрено-блокаторами, сердечными гликозидами, верапамилом (финоптином, изоптином). После отмены этих препаратов атриовентрикулярная проводимость нормализуется.
Атриовентрикулярная блокада II ст. I типа Мобитца (с периодами Венкебаха) возникает у 4-10% больных инфарктом миокарда. Данный тип атриовентрикулярной блокады обусловлен ишемией атриовентрикулярного узла и чаще обнаруживается при диафраг-мальном (нижнем) инфаркте миокарда, носит обычно преходящий характер, практически не влияет на прогноз и не требует специального лечения. Как правило, эта блокада проходит самостоятельно в течение 24–48 ч, но иногда может отмечаться в течение нескольких суток.
Атриовентрикулярная блокада II ст. II типа Мобитца наблюдается менее чем у 1% больных инфарктом миокарда, чаще всего при локализации в передней стенке левого желудочка. При этом замедление проводимости происходит в нижних отделах ствола пучка Гиса. Как правило, изменения носят необратимый характер. Этот тип блокады может сопровождаться выраженной брадикар-дией (при частом регулярном выпадении желудочковых комплексов), возможно внезапное развитие полной атриовентрикулярной блокады. Наиболее часто полная атриовентрикулярная блокада развивается у больных с удлиненным интервалом Р(5 в сочетании с полной блокадой левой ножки пучка Гиса или с блокадой правой и ветвей левой ножки пучка Гиса.
Если атриовентрикулярная блокада II ст. II типа Мобитца характеризуется выраженной брадикардией и, в особенности, если она сочетается с передним инфарктом миокарда, блокадой ножки пучка Гиса, необходимо срочно производить трансвенозную эн-докардиальную электрокардиостимуляцию (кардиостимулятором типа «деташЗ», т. е. функционирующего только при снижении ЧСС ниже определенной, фиксированной для данного пациента величины 50–70).
При нижнем инфаркте миокарда с нерасширенными желудочковыми комплексами, нормальной ЧСС, отсутствием признаков недостаточного кровоснабжения жизненно важных органов электрокардиостимуляцию не проводят, но важным является нахождение больного под постоянным наблюдением. В случае замедления ЧСС, снижения АД, появления стенокардии и головокружений производится электрокардиостимуляция.
Атриовентрикулярная блокада III ст. (полная атриовентрикулярная блокада) развивается в 5–8% случаев при инфаркте миокарда.
При поражении ветви правой коронарной артерии, снабжающей кровью атриовентрикулярный узел, полная атриовентрику-лярная блокада сочетается с инфарктом миокарда задненижней стенки левого желудочка. При этом полной блокаде предшествует атриовентрикулярная блокада I ст. или блокада II ст. типа Мо-битцЛ, водитель ритма желудочков расположен в атриовентри-кулярном узле. Приблизительно у 70% больных ЧСС превышает 40 ударов в 1 мин, не возникают приступы Морганьи-Адамса– Стокса, комплексы С›К8 не расширены. Этот вид блокады может исчезнуть в течение нескольких дней. Летальность при этом варианте блокады составляет около 15%.
При поражении ветви левой коронарной артерии, которая снабжает кровью левожелудочковую перегородку, развивается инфаркт передней стенки левого желудочка и переднеперегородочной области. При этом полная атриовентрикулярная блокада возникает внезапно в первые сутки, ЧСС составляет менее 40 ударов в минуту, возникают приступы Морганьи-Адамса-Стокса, комплекс 01К8 расширен и деформирован (водитель ритма находится ниже бифуркации пучка Гиса). При этом типе блокады часто развивается тяжелая левожелудочковая недостаточность, возможен и кардио-генный шок. При полной атриовентрикулярной блокаде с широкими комплексами ОД8 у больных инфарктом миокарда передней стенки летальность достигает 80% (А. Л. Сыркин, 1991 г.).
При развитии полной атриовентрикулярной блокады в первые часы от начала инфаркта миокарда в ее происхождении может иметь значение высокий тонус блуждающего нерва (обычно это блокада с частотой сокращений желудочков более 40 в минуту, с узкими комплексами ОД8). Такая блокада, как правило, исчезает в первые несколько часов или суток.
Лечение полной атриовентрикулярной блокады заключается в следующем.
1. Если при полной атриовентрикулярной блокаде число сокращений желудочков составляет 40–60 в минуту, нет нарушений гемодинамики и комплексы СЯК8 на ЭКГ не расширены, то специальное лечение не проводится. Этот вид блокады чаще наблюдается при задненижнем инфаркте миокарда и в некоторых случаях исчезает самостоятельно.
2. Если у больного имеется передний инфаркт миокарда с полной атриовентрикулярной блокадой с широкими комплексами С)К8 (водитель ритма расположен ниже бифуркации пучка Гиса), но число сокращений желудочков не менее 40 в минуту и нет нарушений гемодинамики, приступов Морганьи-Адамса-Стокса, необходимо только профилактическое введение эндокардиального электрода в полость правого желудочка без проведения кардиостимуляции. Целесообразность превентивного введения таким больным электрода и подключения кардиостимулятора, работающего «по требованию», объясняется возможностью внезапного ухудшения их состояния из-за уменьшения автоматизма желудочкового водителя ритма. Превентивное введение электрода при инфаркте миокарда бывает необходимо также в случае развития бифасци-кулярной внутрижелудочковой блокады и сочетания внутрижелу-дочковой блокады с атриовентрикулярной блокадой I–II ст.
3. Основным методом лечения полной атриовентрикулярной блокады при инфаркте миокарда является эндокардиальная кардиостимуляция.
Показаниями для проведения электрокардиостимуляции являются: редкий ритм желудочковых сокращений (менее 40 в минуту) при отсутствии эффекта от медикаментозной терапии; приступы Морганьи-Адамса-Стокса; появление признаков левожелудоч-ковой недостаточности; артериальная гипотензия.
4. Медикаментозная терапия, направленная на ускорение ритма желудочков, проводится при появлении показаний для ускорения ритма желудочков (т. е. уменьшении числа сокращений желудочков менее 40–50 в минуту, артериальной гипотензии, при начальных проявлениях левожелудочковой недостаточности, приступах Морганьи-Адамса-Стокса), отсутствии возможности произвести эндокардиальную электростимуляцию, а также для ускорения ритма желудочков можно применять следующие лекарственные средства.
Атропин – периферический М-холинолитик, понижает тонус блуждающего нерва, вводится внутривенно или подкожно в дозе 0,6–0,75 мл 0,1%-ного раствора 3–4 раза в сутки. Эффект от лечения атропином наблюдается нечасто.
Изадрин – стимулятор в-адренорецепторов миокарда, повышает активность идиовентрикулярного водителя ритма. Рекомендуется внутривенное капельное введение препарата (1 мг препарата растворяется в 250 мл 5%-ного раствора глюкозы, вводится со скоростью 0,25 мл/мин). При отсутствии изадрина для внутривенного введения можно воспользоваться приемом изадрина в таблетках под язык (по 1 таблетке каждые 2 ч до учащения ритма желудочков). После достижения частоты сокращения желудочков 50–60 в минуту можно перейти к приему алупента внутрь в дозе 0,02 г каждые 6 ч.
Алупент, или астмопент – стимулятор в-адренорецепторов, повышает активность идиовентрикулярного водителя ритма, вводится внутривенно по 1 мл 0,05%-ного раствора в 20 мл изотонического раствора натрия хлорида 2–3 раза в день с последующим переходом на прием внутрь по 0,02 г каждые 4–6 ч.
При лечении стимуляторами в-адренорецепторов необходимо контролировать уровень АД и ЭКГ (возможно появление желудочковой экстрасистолии). Дозу в-адреномиметиков необходимо подбирать так, чтобы не было экстрасистол или их количество не превышало 2 за 1 мин.
Лечение при нарушениях внутрижелудочковой проводимости Приблизительно у 15–20% больных инфарктом миокарда развивается блокада ножек или ветвей левой ножки пучка Гиса.
Полная блокада правой ножки пучка Гиса регистрируется у 2% больных, но в 40–45% случаев может перейти в полную атрио-вентрикулярную блокаду, при этом летальность может достигать 46%. Полная блокада левой ножки пучка Гиса развивается у 2–5% больных и в 20% случаев может привести к развитию полной атриовентрикулярной блокады, сопровождается высокой летальностью (около 45%).
Блокада левой передней ветви наблюдается у 3–5% больных инфарктом миокарда, а левой задней ветви – у 1–2%. Изолированная блокада левой задней ветви пучка Гиса наблюдается обычно при обширном инфаркте миокарда и летальность при этом достигает 42%. Блокада правой ножки в сочетании с блокадой задней левой ветви при инфаркте миокарда возникает в 1% случаев, но часто прогрессирует в полную атриовентрикулярную блокаду (более чем в 40% случаев), причем летальность может составить 57%.
Таким образом, блокады ножек пучка Гиса, а также ветвей левой ножки при инфаркте миокарда имеют серьезное прогностическое значение. Особенно плохой прогноз имеют двух– и трех-пучковые блокады.
Основным лечебным мероприятием при блокадах ножек пучка Гиса является профилактическая, или превентивная, электрокардиостимуляция. Изолированная блокада передней или задней ветви левой ножки пучка Гиса крайне редко осложняется полной атриовентрикулярной блокадой и поэтому не требует профилактической электрокардиостимуляции.
Полная блокада правой или левой ножки пучка Гиса, а также блокада правой ножки в сочетании с блокадой передней или задней ветви левой ножки является показанием к профилактической установке электрокардиостимулятора.
При трехпучковой блокаде лечебная тактика та же, что и при полной атриовентрикулярной блокаде.
Чрезвычайно важным остается вопрос о показаниях к временной эндокардиальной электрокардиостимуляции при инфаркте миокарда. У некоторых больных, при наличии показаний, профилактически используются наружные кардиостимуляторы.
Лечение хронической ишемической болезни сердца у пожилых пациентов очень часто сочетается с другой важной кардиологической проблемой – лечением сердечных аритмий. С одной стороны, сердечные аритмии в большинстве случаев возникает на фоне хронической ишемической болезни сердца, с другой, они оказывают существенное влияние на ее течение и прогноз, ухудшая их, в ряде случаев являясь непосредственной причиной смерти. Все это диктует необходимость их лечения.
К сердечным аритмиям, требующим обязательного лечения, относят пароксизмальные тахикардии, желудочковые и суправен-трикулярные, полную атриовентрикулярную блокаду, дисфункцию синусового узла с асистолией более 3–5 с. К прогностически неблагоприятным относят также частую пароксизмальную фибрилляцию предсердий, желудочковые экстрасистолии высоких градаций по классификации Лауна.
Многолетние наблюдения ученых позволяют сделать вывод, что у пациентов пожилого возраста наиболее часто встречается фибрилляция предсердий, желудочковая экстрасистолия высоких градаций, синдром слабости синусового узла.
Фибрилляция предсердий у большинства пациентов начинается с пароксизмов различной продолжительности и темпа сокращений предсердий. На ранних этапах желательно купировать пароксизмы фибрилляции предсердий, используя для этого различные противоаритмические препараты. В медицинской литературе даны рекомендации к их применению. Некоторые пациенты со временем начинают улавливать по ощущениям пароксизм фибрилляции предсердий и в первые же минуты принимают внутрь один из препаратов, самостоятельно купируя пароксизм. После восстановления синусового ритма целесообразно продолжение приема противоаритмического препарата для предупреждения возможного рецидива фибрилляции предсердий. В практике, как правило, используется препарат, купирующий пароксизм, а при его неэффективности – какой-либо другой. Наиболее часто применяются следующие препараты: амиодарон, пропафенон, атенолол, дизопир-амид, хинидин. Доза препаратов, длительность противорецидивного курса лечения подбираются индивидуально, но у пожилых пациентов должны быть минимальными.
Среди нарушений сердечного ритма, имеющих большое значение для врача общей практики, по контингенту лиц пожилого возраста является синдром слабости синусового узла, обозначаемый в литературе также терминами «болезнь синусового узла», «дисфункция синусового узла». На раннем этапе синдром слабости синусового узла проявляется эпизодами немотивированной общей слабости, головокружением. Позднее присоединяется прогрессирующая брадикардия, синдром «тахибради», пароксизм фибрилляции предсердий. Но основным симптомом являются эпизоды асистолии 3–5 с и более. Для подтверждения синдрома слабости синусового узла можно проводить пищеводную электростимуляцию предсердий. Но в практическом здравоохранении ограничиваются суточным мониторированием ЭКГ, во время которого выявляются эпизоды асистолии по удлинению интервала R-R. Многолетние попытки лечения синдрома слабости синусового узла лекарственными препаратами не давали желаемого результата, и больные умирали, как правило, от прогрессирующей сердечной недостаточности. Поэтому сегодня единственным эффективным методом лечения, улучшающим состояние и способствующим сохранению жизни больного, является постоянная электростимуляция сердца, причем целесообразно осуществлять ее как можно раньше. Никаких возрастных ограничений для имплантации электростимулятора нет, при этом пациенты могут вести активный образ жизни.
Немедикаментозные методы лечения
Хотя роль немедикаментозных методов лечения у пожилых пациентов значительно меньше, чем у лиц молодого возраста, но назначение им дозированных лечебных нагрузок (ЛФК, ходьба в среднем темпе), лечебного массажа, некоторых физиотерапевтических процедур (сухие углекислые ванны) целесообразно. В реабилитационном периоде может проводиться гипербаротерапия. Назначается курсами по 8-10 процедур, каждая продолжительностью 40 мин, в режиме до 1 избыточной атмосферы пациентам с хронической ишемической болезнью сердца, сочетающейся с другими заболеваниями (диабетическая микроангиопатия, дисциркуляторная энцефалопатия, пептическая язва желудка). Каких-либо осложнений не наступает, дозу лекарственных препаратов в 50% случаев удается снизить.
Лечение тромбоэмболических осложнений
Тромбоэмболические осложнения при инфаркте миокарда клинически диагностируются у 10% больных, однако при аутопсии частота их выявления достигает 45%, что свидетельствует о частом бессимптомном течении тромбоэмболий. Тромбоэмболические осложнения могут стать причиной смерти больных инфарктом миокарда. Одним из наиболее опасных для жизни тромбоэмболиче-ских осложнений является тромбоэмболия легочной артерии. При инфаркте миокарда могут наблюдаться также тромбоэмболии артерий большого круга кровообращения. Тромбоэмболия церебральных артерий может быть причиной инсульта, селезеночной артерии – инфаркта селезенки, почечной артерии, следствием этого является инфаркт почки. Возможна также тромбоэмболия артерий нижних конечностей. Около 30% больных инфарктом миокарда с акинезией или дискинезией передневерхушечной зоны миокарда имеют внутри желудочковые тромбы. Однако большая часть тромбов остается неподвижной, поэтому эмболии в артерии большого круга наблюдаются редко.
Лечение тромбоэмболических осложнений при инфаркте миокарда заключается, прежде всего, в гепаринотерапии. При отсутствии противопоказаний в течение 5–7 дней проводится лечение гепарином – вначале 10,000 ЕД внутривенно струйно, затем по 1000 ЕД/ч или по 5000–7000 ЕД каждые четыре часа под контролем частичного активированного тромбопластинового времени. Терапевтическая доза гепарина соответствует увеличению этого показателя в 1,5–2,5 раза по сравнению с исходным. В дальнейшем гепарин постепенно отменяют, за 3–5 дней до его отмены назначаются антикоагулянты непрямого действия, лечение которыми продолжается около трех месяцев под контролем протром-бинового времени (при оптимальной дозе антикоагулянтов про-тромбиновый индекс должен быть в пределах 50–60%). Однако в последние годы некоторые специалисты предлагают вместо непрямых антикоагулянтов применять длительно действующие ан-тиагреганты (аспирин в малых антиагрегантных дозах, тиклопидин).
При развитии тромбоэмболии артерий конечностей производят эмболэктомию, если позволяет общее состояние больного. Операция проводится под местной анестезией с использованием катетера Фогарта.
Лечение ранней постинфарктной стенокардии
Ранней постинфарктной стенокардией обозначается стенокардия, развивающаяся в течение первых двух недель (по некоторым данным, в течение 3–4 недель) после развития инфаркта миокарда. Ранняя постинфарктная стенокардия относится к группе нестабильной стенокардии, является неблагоприятным прогностическим признаком. Лечение ранней постинфарктной стенокардии проводится следующим образом.
1. Больному рекомендуется полупостельный режим, разрешается пользоваться туалетом. Больной должен находиться под мони-торным наблюдением.
2. Назначается необременительное гипокалорийное питание (1500 ккал в сутки). Необходимо нормализовать стул больного.
3. Необходимо создать благоприятную психоэмоциональную обстановку, вселяющую уверенность в выздоровлении. Целесообразен прием с этой целью небольших доз седативных препаратов (диазепам, элениум и др.).
4. Бета-адреноблокаторы (пропранолол или другие) назначаются только после того, как установлено отсутствие у больного противопоказаний к их применению: левожелудочковой недостаточности, бронхиальной астмы, хронического обструктивного бронхита, нарушений атриовентрикулярной проводимости. Нецелесообразным считается применение β-адреноблокаторов при типичной стенокардии покоя, так как стенокардия в этом случае может быть обусловлена спазмом коронарных артерий. В такой ситуации из антиангинальных средств назначаются только нитраты и антагонисты кальция. Дозу препарата постепенно увеличивают до тех пор, пока не будет достигнут адекватный уровень блокады в-адреноре-цепторов (ЧСС менее 55-100). Суточная доза пропранолола вначале составляет 20–40 мг 3 раза в день, в дальнейшем она может быть увеличена до 40–80 мг 3–4 раза в день.
5. Одновременно с β-адреноблокаторами назначаются нитраты – изосорбида динитрат по 5-20 мг под язык или для разжевывания каждые четыре часа. Можно использовать накожно нитроглицериновую мазь, начальная доза обычно составляет 1,5 см каждые 4–6 ч. Дозировка может быть увеличена до 5 см каждые 4 ч в период бодрствования больного. Мазь наносят на участки кожи площадью 15 см X 15 см. Вместо мази можно использовать нитроглицериновые диски-наклейки. Комбинированная терапия в-адреноблокаторами и нитратами должна осуществляться под контролем уровня АД и не должна допускать снижения систолического АД ниже 90-100 мм рт. ст. Многие кардиологи при выраженных болях в области сердца одновременно с вышеназванными препаратами назначают нитроглицерин внутривенно капельно.
6. При сохранении эпизодов стенокардии покоя, плохой переносимости нитратов к проводимой терапии добавляются антагонисты кальция (нифедипин – 10–40 мг 3–4 раза в сутки). Однако антагонисты кальция не должны назначаться, если имеются признаки снижения сократительной способности миокарда.
7. Проводится лечение гепарином и антиагрегантными дозами аспирина.
8. При повторяющихся эпизодах нестабильной стенокардии больным может проводиться коронарная ангиография, а в последующем аортокоронарное шунтирование или баллонная ангиопластика. Обычно хирургическое лечение проводится не ранее чем через 3–4 недели после начала инфаркта миокарда. Однако при тяжелом течении стенокардии оперативное лечение возможно и в более ранние сроки.
Лечение артериальной гипертензии
Артериальная гипертензия оказывает отрицательное влияние на течение инфаркта миокарда, так как повышает постнагрузку на миокард и потребности миокарда в кислороде, повышает риск развития аневризмы и разрыва сердца. Рекомендуется следующая тактика лечения артериальной гипертензии при инфаркте миокарда.
1. Постельный режим, лечение болевого синдрома, седативная терапия.
2. Лечение β-адреноблокаторами. Эти препараты назначают в начале терапии внутривенно в малых дозах, а затем, при хорошей переносимости, внутрь.
3. Внутривенное капельное введение натрия нитропруссида. Лечение данным препаратом показано при выраженной артериальной гипертензии, вызывает быстрое снижение АД в результате венозной и артериальной вазодилатации. Инфузию начинают с дозы 10–15 мкг/мин, в дальнейшем скорость увеличивают на 5– 10 мкг/мин каждые 5-10 мин до достижения гипотензивного действия.
4. Внутривенное введение нитроглицерина. Вызывает венозную и умеренную артериолярную дилатацию, снижение АД. Этот метод лечения особенно показан при артериальной гипертензии на фоне стенокардии и сердечной недостаточности, а также, если у больного долго сохраняются явления ишемии миокарда на электрокардиограмме. Инфузию начинают со скоростью 10 мкг/мин, повышая ее на 5-10 мкг/мин каждые 5-10 мин до нормализации АД.
5. Целесообразно применять ингибиторы АПФ (капотен по 12,5– 25 мг 2–3 раза в день; эналаприл 2,5-10 мг 1 раз в день, при необходимости можно повысить дозу до 20 мг в сутки).
Антагонисты кальция при инфаркте миокарда в настоящее время не применяются, так как выявлено их неблагоприятное влияние на прогноз.
Дозированные физические нагрузки
Физическая реабилитация и кинезотерапия – трудный и наиболее специфический аспект реабилитации. Основные виды физической реабилитации: дозированная ходьба, лечебная гимнастика, занятие в тренажерном зале. Объем нагрузок постоянно контролируется врачом лечебной физкультуры и лечащим врачом. Методисты по лечебной физкультуре обучают больных контролю адекватности их физических нагрузок, целесообразности умеренных нагрузок (не более 60% от максимальной индивидуальной переносимости). Результаты теста толерантности к физическим нагрузкам являются основой построения реабилитационной программы. Вначале больного обучают выполнению физических упражнений, подтверждают их безопасность, убеждаются в положительном эффекте тренировок. Квалификация, опыт работы методиста по лечебной физкультуре позволяет планировать организацию на базе санатория школы методистов по лечебной физкультуре. Эффективность реабилитации больных, перенесших инфаркт миокарда, определяется точным знанием перспектив восстановительного лечения, правильностью подбора индивидуальной программы реабилитации, тщательностью их выполнения, адекватностью контроля, динамикой клинико-функ-ционального состояния больного. Индивидуальные программы физической реабилитации – эффективный инструмент повышения РП, обеспечения максимально возможной реинтеграции больного в общество и достижения оптимального качества жизни.
Самой трудной задачей физической реабилитации является определение уровня допустимых нагрузок с точки зрения безопасности. Необходимо учитывать степень дезадаптации больного и влияние медикаментозных препаратов, влияющих на гемодинамику.
Так, у больных с хронической сердечной недостаточностью используется тест с 6-минутной ходьбой при поступлении и перед выпиской на амбулаторное лечение для определения тренирующего эффекта, полученного в процессе кинезотерапии и комплекса реабилитационных мероприятий.
Основные эффекты лечебного действия физической реабилитации следующие: тонизирующий эффект; трофическое (метаболическое) действие; формирование компенсации; нормализация функций (тренирующий эффект); психотерапевтическое действие.
Существует несколько этапов, или фаз, физической реабилитации пациентов после перенесенного инфаркта миокарда.
Острая фаза начинается, когда после нескольких дней болезни у больного улучшается состояние и остается лишь небольшое количество жалоб, связанных с заболеванием сердца. Пациент при этом соблюдает постельный режим.
Фаза выздоровления начинается, когда человек окончательно встает с постели, способен стоять, ходить и подниматься на один пролет лестницы. Обычно в это время пациента выписывают из больницы. Эта фаза заканчивается функциональным максимальным выздоровлением, примерно в это время человек возвращается к своей работе.
Фаза после выздоровления, или поддерживающая, продолжается в течение всей остальной жизни.
Основными целями реабилитации больных, перенесших инфаркт миокарда, на диспансерно-поликлиническом этапе являются завершение периода временной нетрудоспособности, восстановление трудоспособности, проведение мероприятий по вторичной профилактике ИБС.
На санаторном этапе физическая реабилитация строится с учетом класса тяжести инфаркта миокарда, при этом используются лечебная гимнастика, дозированная ходьба, тренировочная ходьба по лестнице с постепенным увеличением интенсивности физических нагрузок. В отделение реабилитации местных санаториев переводятся больные с I–III классами тяжести заболевания при удовлетворительной адаптации их к IV ступени двигательной активности.
Противопоказаниями для направления в санаторий являются:
1) общие противопоказания для направления в санаторий (острые инфекционные заболевания, венерические заболевания, психические и онкологические заболевания, болезни крови в острой стадии и стадии обострения);
2) недостаточность кровообращения ПБ ст. и выше;
3) тяжелые степени нарушения сердечного ритма и проводимости;
4) тяжелые степени коронарной недостаточности;
5) рецидивирующее течение инфаркта миокарда;
6) гипертоническая болезнь ПБ-III ст.;
7) аневризма сердца (острая или хроническая) с явлениями недостаточности кровообращения выше I ст.;
8) аневризма аорты;
9) нарушения мозгового кровообращения в острой или подост-рой стадии;
10) рецидивирующие тромбоэмболические осложнения;
11) декомпенсированный сахарный диабет.
На санаторном этапе физическая реабилитация строится с учетом класса тяжести заболевания, при этом широко используется лечебная гимнастика, дозированная ходьба, тренировочная ходьба по лестнице с постепенным увеличением интенсивности физических нагрузок. Необходимо добиваться адекватной реакции на физическую нагрузку, что достигается в среднем через 2–6 недель физических тренировок, которые развивают коллатеральное кровообращение.
Цель: адаптация организма к физическим нагрузкам.
При лечении инфаркта миокарда лечебная физкультура базируется на принципе точного подбора упражнений, постепенности и дозированности нагрузки, очередности применения упражнений, соответствующей лечебно-восстановительной последовательности, смене одних упражнений другими по мере достижения улучшения. Восстановительные упражнения должны точно соответствовать форме и стадии развития заболевания. Двигательные упражнения в форме дозированного усиления чаще всего воспринимаются как дополнительная нагрузка на организм. В связи с этим они вызывают чрезмерную осторожность. По существу же речь идет о правильной систематизации больных по отношению к лечебным мерам и подборе соответствующего метода кинезотерапии. Установлено, что упражнения, дающие нагрузку больному, одновременно могут приводить к разгрузке пораженного органа. Например, вызвав гиперемию на периферии, мы тем самым разгрузим сердечную мышцу. Осознание такой зависимости методистом и больным обеспечивает хорошие результаты двигательного восстановления. Ни максимальная нагрузка, ни ограничение нагрузки до минимума не приведет к поставленной цели. Реабилитолог подбирает для больных, перенесших инфаркт миокарда, оптимальную индивидуальную нагрузку.
Инфаркт успешно лечиться только в том случае, если пациент будет не пассивно болеть, а помогать врачу в борьбе с недугом. Больному нельзя уходить в болезнь. Спокойное хорошее настроение, положительные эмоции способствуют быстрейшему заживлению поврежденной мышцы сердца, нормализации ее работы.
Инфаркт влечет за собой увеличение слабости, снижение силы, возбуждает беспокойство и обусловливает пессимизм. Все эти элементы, поддерживаемые всеобщей ошибочной убежденностью во вредности и опасности для жизни физической нагрузки, ведут и к ошибочной тактике избегать движения, исключать все формы активной жизни, а в конечном итоге, возникает мышечная атрофия, нарушение координации. В реабилитационную программу ЛФК входят: дозированная, специальная физическая нагрузка, дыхательные упражнения, специальные энергетические комплексы упражнений цигун и тай-цзи-цуань, упражнения с предметами.
Необходимо помнить, что для заживления травмированной мышцы сердца нужно время (3–4 месяца), хорошее настроение и определенный режим, который необходимо строго и последовательно соблюдать.
Необходимо также помнить, что продолжительные, внезапные, короткие или непривычные упражнения вредны и даже опасны.
Существует несколько общих правил. Прежде чем пациент приступит к тренировкам, лечащий врач определяет степень его физической активности. От этого будет зависеть интенсивность подходящей для него нагрузки. Есть ряд непременных условий выполнения комплексов лечебной гимнастики.
Заниматься разрешается только при хорошем самочувствии пациента.
При появлении одышки или болей в области сердца необходимо снизить нагрузку или прекратить занятия.
Занятия необходимо проводить в хорошо проветренном помещении.
Одежда больного, перенесшего инфаркт миокарда, должна быть легкой и не стесняющей движения.
Длительность занятий не более 20–30 мин.
Все упражнения следует выполнять без резких движений.
Необходимо соблюдать постепенность и последовательность в увеличении нагрузки.
При выполнении упражнений пациент должен делать вдох через нос, выдох через рот, при этом нельзя натуживаться.
Во время специальных дыхательных упражнений вдох производится плавно, с умеренной глубиной, выдох продолжительнее вдоха; при сочетании дыхания с движением продолжительность вдоха должна соответствовать всей фазе движения (например, руки разводить – вдох, сводить – выдох).
Ходьба по ровному месту дозируется расстоянием, количеством остановок для отдыха, темпом, длительностью всего времени, ушедшего на прогулку.
Сначала необходимо назначить занятия один раз в день, преимущественно утром, затем и во второй половине дня, но не менее чем за два часа до сна. Основной целью тренировок является не достижение атлетических стандартов, а поддержание в течение длительного времени вашего хорошего самочувствия при повседневных нагрузках.
Желательно, чтобы каждый человек, перенесший инфаркт миокарда, имел определенный постоянный маршрут или дистанцию для периодического (но не реже одного раза в неделю) прохождения с целью лучшего наблюдения за увеличением своей тренированности или ухудшением своего состояния.
Чтобы правильно рассчитать свои силы при физической нагрузке, больному необходимо научиться самоконтролю, главным критерием которого является его самочувствие.
Первые несколько дней весьма важно, чтобы во время физических упражнений за пациентом наблюдал его лечащий врач, контролируя при этом пульс, артериальное давление, и, по возможности, записывая электрокардиограмму.
В дальнейшем при хорошей переносимости двадцатиминутной физической нагрузки и после консультации со своим лечащим врачом пациент может довести ее продолжительность до 30 минут в день. Опять же, первые несколько дней повышенной физической активности должны проходить под контролем лечащего врача (см. выше). Во время упражнений пульс должен учащаться. Для вычисления целевого пульса во время упражнений есть специальная формула: из числа 220 нужно вычесть возраст пациента и высчитать 70% от этого числа. Например, если пациенту 50 лет, 220 – 50 = 170. 70% от 170 = 119. Поэтому, чтобы извлечь максимальную пользу из физических упражнений, пятидесятилетнему пациенту следует в течение 30-минутных занятий поддерживать свой пульс на уровне 119 ударов в минуту. Однако при этом пациент должен чувствовать себя комфортно и, конечно же, у него не должно возникать никаких кардиологических жалоб.
При появлении увеличения интенсивности болей в области сердца, в груди (независимо от данных ЭКГ), сильной одышки, холодного пота, учащения пульса – более 120 ударов в минуту, общей слабости больному необходимо немедленно прекратить физические нагрузки и далее вести себя как при приступе стенокардии. Впоследствии необходимо сообщить об ухудшении состояния лечащему врачу.
Некоторые больные ошибочно полагают, что, если при физической нагрузке возникают недомогание или боль в области сердца, не следует прекращать занятий и боль надо пересилить. Необходимо убедить пациента в том, что это опасное заблуждение может привести к трагическим последствиям.
Существует и другая крайность, когда человек, перенесший инфаркт, целиком уходит в болезнь и боится любой, даже самой незначительной, физической нагрузки. Подобное поведение является также неправильным. Это объясняется тем, что стенокардия появляется тогда, когда потребность сердечной мышцы в кислороде не удовлетворяется из-за неспособности артерий сердца его доставлять. Специально подобранные лечащим врачом физические упражнения, выполняемые в медленном темпе, дыхательная гимнастика способствуют продвижению крови по артериям и венам, что облегчает работу сердца, улучшает обмен веществ, повышая отдачу кислорода и питательных веществ тканям, нормализуют работу всех органов. Под влиянием физических тренировок отмечается ряд положительных эффектов: повышается физическая работоспособность, нормализуется кровяное давление, улучшается эластичность сосудов и снижается в крови концентрация веществ, способствующих возникновению атеросклероза. Значительно улучшается психологическое состояние, настроение, исчезает страх физической нагрузки, появляется уверенность в своих силах.
Сложность реабилитации после перенесенного инфаркта миокарда заключается и в том, что успех лечения будет зависеть от приверженности самого больного к лечению. Врач в данном случае – лишь советчик и помощник.
Двигательные режимы. Физические тренировки начинаются еще на этапе лечения в стационаре. Начинаются с тренировок малых мышечных групп. Можно начинать с занятий, направленных на разработку мышц кистей рук. Занятия проводятся с 3–8 дня болезни.
Тренировки кистей рук проводятся в положении сидя на стуле или на краю кровати путем попеременных сжатий резинового эспандера правой и левой руками. Начальная интенсивность нагрузки – 40 попеременных сжатий эспандера правой и левой руками в минуту, длительность – 10 мин. После завершения физических тренировок малых мышечных групп для верхних конечностей больному предлагается выполнение тренирующих упражнений с использованием эспандеров для ног в том же объеме. Физическая тренировка малых мышечных групп проводится ежедневно. При хорошей переносимости через каждые два дня интенсивность физических тренировок увеличивается на 10 сжатий эспандера в минуту. Продолжительность занятий – 10 мин. Максимальная интенсивность физической тренировки малых мышечных групп на стационарном этапе не должна превышать 100 попеременных сжатий эспандера в минуту правой и левой конечностями.
Физические тренировки малых мышечных групп проводятся под руководством и контролем методиста лечебной физкультуры. ЧСС и АД во время тренировки определяются каждые 5 мин. Выполнение упражнений следует прекратить при увеличении систолического АД более чем на 40 мм рт. ст., диастолического – на 15 мм рт. ст., ЧСС на 30 мин и более по сравнению с исходными показателями или урежении пульса на 10 ударов в минуту.
Физические тренировки малых мышечных групп проводятся ежедневно в течение периода освоения II ступени физической активности.
После перевода больного на III ступень физической активности физические тренировки малых мышечных групп рекомендуется проводить два раза в неделю, чередуя с другими элементами физических тренировок (дозированная ходьба).
Комплекс физических тренировок больных инфарктом миокарда продолжается и на IV ступени физической активности, вплоть до выписки из стационара.
Во время упражнений пульс должен учащаться. Дозированная ходьба – составная часть программы физических тренировок на стационарном этапе. Л. М. Аронов (1988 г.) для определения индивидуального тренировочного темпа ходьбы с учетом толерантности больного к физической нагрузке предлагает пользоваться следующей формулой:
X = 0,042W + 0,15n+ 65,555
где X – искомый темп ходьбы (число шагов в минуту); W – мощность последней ступени нагрузки при ВЭМ (в кг/м/мин); п – ЧСС на высоте нагрузки в минуту. За величину W берется мощность последней ступени нагрузки в том случае, если больной выполнял ее в течение не менее 3-х мин. Дозированная ходьба проводится вначале под контролем методиста ЛФК. В дальнейшем больной сам контролирует свой пульс. Частоту пульса следует поддерживать на уровне не выше 95% пороговой.
Расстояние при дозированной ходьбе определяется уровнем пороговой мощности. При пороговой мощности 50 Вт больным предлагается проходить до 3 км в день за 3–6 приемов, при пороговой мощности выше 50 Вт – 5 км за 5-10 приемов.
Первый двигательный режим называется щадящим, так как он предусматривает малую физическую активность. Данный двигательный режим применяется для больных, перенесших инфаркт миокарда 2–4 месяца назад, а также для больных с выраженными явлениями коронарной недостаточности, недостаточности кровообращения 2-й степени.
В этот режим входят два комплекса упражнений № 1 и № 2. Комплекс № 2 является переходным к следующему режиму.
Выполнять комплексы следует строго не более 15–20 мин. Помимо этого во время 1-го двигательного режима предусматриваются тренировочные подъемы по лестнице. В первую неделю людям, перенесшим инфаркт миокарда, рекомендуется подниматься в медленном темпе до 2-го этажа (1 ступенька в течение 3–4 с), дыхание произвольное. На 2-й неделе, поднявшись на 2-й этаж, необходимо остановиться, 4–5 раз глубоко вдохнуть и выдохнуть, затем, если нет одышки, общей слабости и резкого учащения пульса, постараться продолжить подъем до 3-го этажа. Когда больной привыкнет к такой нагрузке, можно начать подниматься по лестнице 2 раза в день в среднем темпе (1 ступенька – 2 с). Количество тренировок в день постепенно доводиться до 3–4. Кроме того, можно начинать дозированные прогулки. На первой неделе больной проходит расстояние в 1 км за 30 мин. На второй неделе необходимо увеличить прогулку до 1,5 км с той же скоростью. На третьей неделе до 2 км, на четвертой неделе – 2,5 км (при той же скорости ходьбы). После каждого километра необходимо отдыхать 5-10 мин. Начиная с третьей недели, необходимо ходить по 2 раза в день; вечером рекомендуется проходить половину расстояния.
При первом двигательном режиме сложно выполнять некоторые виды кратковременных домашних работ с незначительным физическим усилием, подъем тяжестей до 5 кг.
Показаниями для перехода к следующему режиму являются самочувствие пациента, адаптация его к физической нагрузке, хорошие показатели кардиограммы.
Второй двигательный режим иначе называется тренировочным со средней физической активностью. Он может быть рекомендован тем, кто перенес инфаркт миокарда четыре и более месяцев назад и успешно освоил первый двигательный режим, а также больным с сердечно-сосудистой недостаточностью I степени. Тренировочный режим включает в себя более интенсивные нагрузки. В его комплексы входят упражнения для усовершенствования координации движений, для активизации кровообращения и дыхания, для поднятия эмоционального тонуса, для восстановления и сохранения привычки сердечно-сосудистой системы к выполнению нормальных бытовых нагрузок. Этот режим предусматривает упражнения с отягощением, и рекомендуемая нагрузка до 2–3 кг. Длительность выполнения упражнений не должна превышать 25–30 мин. Главная цель этого этапа – развить приспособляемость сердечно-сосудистой системы и всего организма к физическим бытовым нагрузкам.
При этом режиме перенесший инфаркт миокарда человек может продолжать тренироваться, поднимаясь по лестнице. В первую неделю допускается делать это в среднем темпе – 1 ступенька за 2 с – до 2-го этажа, затем отдых 2–3 мин и снова продолжение подъема в том же темпе до 3-го этажа. На следующей неделе – подъем до 4-го этажа этим же темпом. Спускаться по лестнице надо с той же скоростью, как и подниматься. Количество тренировок в день можно довести до 3-4-х.
Дозированной ходьбой можно рекомендовать заниматься дважды в день 2–3 раза в неделю. Вечером рекомендуется проходить половину расстояния. Начиная с дистанции 2,5–3 км, увеличивайте ее каждую неделю на 500 м, доведя к четвертой неделе занятий до 4,5–5 км. На первой неделе рекомендуется медленный темп ходьбы, затем увеличение скорости. Периоды ходьбы в среднем темпе нужно чередовать с ходьбой в более медленном темпе. После каждых 1,5 км необходимо отдыхать 5-10 мин.
В этот период разрешается немного помогать домашним: делать мелкий ремонт и уборку в квартире, ходить в магазин, поднимая сумки не тяжелее 5 кг.
Итак, если человек, перенесший инфаркт миокарда, успешно прошел два предыдущих режима, можно перевести его к третьему. Большинство людей, успешно завершив его, возвращаются к нормальной трудовой жизни. Главная задача этого режима – максимально обеспечить восстановление трудоспособности организма больного.
Продолжительность выполнения упражнений возрастает до 35–45 мин. В течение этого режима можно по 10–15 мин играть в волейбол, в настольный теннис, бадминтон. Можно начинать плавать в бассейне, но после согласования с лечащим врачом.
Обязательно продолжать тренироваться в подъеме по лестнице. В первую неделю придерживайтесь среднего темпа подъема (30 ступенек за 1 мин), один раз в день. Затем постепенно увеличивайте длительность и периодически темп.
Дистанция дозированной ходьбы во время этого режима начинается с 5–5,5 км и еженедельно постепенно увеличивается на 500 м, доходя на четвертой неделе тренировок до 8–8,5 км. Скорость ходьбы – 4 км/час, после каждых 2 км отдыхайте 5-10 мин. Вы можете начинать ходить по дороге с незначительными подъемами, постепенно ускоряя темп.
Лечебная гимнастика
В реабилитации больных, перенесших инфаркт миокарда, первостепенная роль отводится лечебной гимнастике. Занятия лечебной гимнастикой проводятся в трех залах и в четырех тренажерных залах с богатым набором тренажеров. Классификация степени тяжести больных, перенесших инфаркт миокарда, по четырем функциональным классам тяжести, разработанная академиком Д. М. Ароновым, используется врачами-реабилитологами в повседневной практике и при разработке индивидуальных программ.
Кроме функционального класса тяжести, учитывается реабилитационный потенциал (РП). Величина реабилитационного потенциала определяется комплексом медико-социальных, клинико-физиологических компонентов, одними из важнейших компонентов которого являются достаточный уровень физической активности, которая должна сформироваться к санаторной реабилитации, а также уровень копенсации имеющейся патологии. При I функциональном классе рекомендуются лечебная гимнастика в тренирующем режиме продолжительностью 30–40 мин с ЧСС до 140 мин, занятия в группах здоровья, кратковременное (до 20 мин) участие в спортивных играх (волейбол, ручной мяч, настольный теннис, бадминтон), плавание, ходьба на лыжах, работа по дому (уборка квартиры, небольшой ремонт мебели, квартиры, подъем тяжести до 12–15 кг), работа на садовом участке не более 1–1,5 ч в день, исключая подъем тяжести свыше 12–15 кг, быстрая ходьба (до 110–130 шагов в минуту), кратковременные пробежки (до 1–2 мин) в среднем темпе. Половая активность не ограничивается. При II функциональном классе рекомендуются лечебная гимнастика в щадяще-тренирующем режиме продолжительностью не более 30 мин с ЧСС на высоте нагрузки до 130 в минуту, занятия в специальных группах длительных физических тренировок по программе «сильной» группы с ЛФК, элементами спортивных игр, тренировками на ВЭМ, кратковременные (до 10 мин) несостязательные спортивные игры (волейбол, настольный теннис, бадминтон), плавание в бассейне, дозированная ходьба на лыжах, разрешается работа по дому (уборка квартиры, приготовление пищи, поднятие тяжести до 6–8 кг), работа на садовом участке, за исключением обработки почвы лопатой, подъема и переноски тяжестей более 8 кг, умеренная ускоренная ходьба (до 110 шагов в минуту) и кратковременная (по 2–3 мин) быстрая ходьба в темпе 120–130 шагов в минуту, кратковременные пробежки в умеренном темпе (до 1–2 мин). Половая активность не ограничивается. При III функциональном классе рекомендуются ЛФК в щадяще-тренирующем режиме продолжительностью не более 30 мин с ЧСС на высоте нагрузки до 110 в минуту, занятия в группах длительных физических тренировок по программе «слабой» группы. Спортивные игры, плавание, ходьба на лыжах противопоказаны. Разрешаются ходьба в среднем темпе (до 80–90 шагов в минуту), легкие виды домашних работ. Половая активность ограничивается. При IV функциональном классе активная физическая реабилитация противопоказана. Больным рекомендуется ЛФК в щадящем режиме, разрешается частичное самообслуживание. Для ускорения процесса выздоровления после перенесенного инфаркта миокарда необходимо проводить аэробные физические нагрузки, которые способствуют насыщению крови кислородом, их длительность составляет 20 мин. Аэробные нагрузки способствуют работе разнообразных групп мышц с заданной силой. В таком упражнении участвуют несколько крупных групп мышц, для них сердце и легкие осуществляют подачу кислорода. Это упражнение увеличивает сердечную и физическую выдержку, оно включает: спортивную ходьбу на тренажере «бегущая дорожка», где используется различная степень сложности, велотренажер, а также ходьба вокруг спортзала и плавание. Известно, что регулярные физические нагрузки динамического типа снижают риск возникновения различной сердечно-сосудистой патологии. Риск развития смертельного исхода от ишемической болезни сердца у людей, которые каждый день в течение 20 мин занимаются физическими упражнениями небольшой степени интенсивности, на 30% ниже такого же показателя у людей, ведущих малоподвижный образ жизни. Этот положительный эффект имеет связь с возможностью физической нагрузки влиять на артериальное давление, так как вызывает его снижение. Также физические нагрузки способствуют активации ряда метаболических процессов, в том числе они способствуют увеличению содержания «полезного» холестерина (холестерина липопротеидов высокой плотности), а также снижают уровень сахара в крови больных сахарным диабетом.
Значение и возможности снижения избыточной массы тела. При значительном увеличении массы тела на сердце накладывается повышенная нагрузка, также повышается артериальное давление. Поэтому уменьшение массы тела становится необходимой мерой немедикаментозного лечения. Лечащий врач может рекомендовать пациенту программу, которая поможет осуществить снижение избыточной массы тела. Современным показателем, указывающим на успешное осуществление мер по борьбе с избыточным весом, является такой показатель, как индекс массы тела (ИМТ). Он рассчитывается как отношение веса (в килограммах) на рост (в метрах) в квадрате (кг/м). У лиц с избыточным весом ИМТ соответствует 25–29,9 кг/м, при выраженном ожирении ИМТ имеет значение свыше 30 кг/м. Лицам с избыточным весом даются рекомендации, где указываются физические тренировки и назначение низкокалорийной диеты. При ожирении назначаются средства, снижающие аппетит или замедляющие всасывание жиров в кишечнике (по назначению врача).
Краткие примечания к применению физических нагрузок, которые имеют связь с садовым участком. Шесть соток для наших соотечественников имеют огромное значение. Садовые или дачные участки – место краткосрочного отвлечения человека от реальной жизни, которая связана с тревогами, проблемами и различными неприятностями городской суеты. С этой точки зрения, имеющиеся у нас загородные участки – это благодать. С другой стороны, эти же участки для многих россиян являются средством к существованию, точнее – пропитанию. А хлеб наш насущный (овощи, фрукты, ягоды, получаемые с наших участков) будет получен только тогда, когда вкладываешь в свою землю много труда, а вернее – здоровья. Необходимо реально оценивать свои возможности, не выходить за рамки того, что рекомендует врач-кардиолог. Необходимо выполнять работу не спеша, с перерывами каждые 20–30 мин. Делать во время работы на садовом участке столько, сколько получается, а не сколько хочется. Необходимо довольствоваться малым, чтобы не допустить потери большего, а это и жизнь, и здоровье. После перенесенного инфаркта миокарда сроки временной нетрудоспособности (ориентировочные) составляют: при мелкоочаговом инфаркте миокарда, протекающем без осложнений – приблизительно 2 месяца; при крупноочаговом (в том числе транс-муральном инфаркте миокарда) – 2–3 месяца; при мелкоочаговом или крупноочаговом осложненном инфаркте миокарда – 3–4 месяца. При рецидивирующем инфаркте миокарда, тяжелых нарушениях ритма и проводимости, выраженной хронической коронарной недостаточности, недостаточности кровообращения ПБ стадии больных направляют на медико-реабилитационную экспертную комиссию, которая или продлевает больничный лист свыше 4 месяцев (если реальна перспектива восстановления трудоспособности), или признает больного нетрудоспособным. При первом функциональном классе больные полностью трудоспособны, но освобождаются от ночных смен, дополнительных работ, командировок. Лица, профессия которых неразрывно связана с тяжелым физическим трудом, переводятся на другую работу. При втором функциональном классе больные трудоспособны, но только в случае, если их работа связана с легким физическим трудом, неинтенсивным физическим напряжением. При третьем функциональном классе больные признаются нетрудоспособными, если их профессия связана с физической нагрузкой и интенсивным психоэмоциональным напряжением. При четвертом функциональном классе больные нетрудоспособны.
Психологическая реабилитация
После прохождения больным стационарного лечения после перенесенного инфаркта миокарда вместе с физическим компонентом имеет большое значение психологический компонент. Существуют разнообразные типы реакции человека на заболевание: от адекватной до ипохондрической. Также велико значение семьи и хороших семейных отношений в периоде адаптации пациента к осуществлению жизнедеятельности вне стационара. Актуальность психологического компонента увеличивается в процессе завершения этапа реабилитации, когда пациент возвращается на рабочее место и происходит восстановление его социального статуса после перенесенного инфаркта миокарда. При успешной и удовлетворительной психической адаптации больные адекватно оценивают свое состояние, следуют рекомендациям врача и стараются вести активный образ жизни. Целью использования психотерапии при лечении инфаркта миокарда становится психологическая адаптация пациентов и ориентация на активный образ жизни. Большое внимание необходимо уделять ликвидации стрессовых, психоэмоциональных причин, которые повлекли развитие инфаркта. В реабилитационную программу входят такие компоненты, как психорегуляция, основанная на рассеянном гипнозе, гетеротренинг, идеомоторные тренировки, адаптационный тренинг, используется также обучение аутотренингу и технике саморегуляции. Со стороны ближайших родственников по отношению к пациенту, который перенес инфаркт миокарда, выявлено три основных типа реакций. В большинстве случаев поведение ближайших родственников основано на чувстве страха за состояние больного, что способствует его чрезмерной опеке, особенно актуально это в вопросах, которые касаются его физической активности. В основном такие родственники находятся около больного при посещении им поликлиники, на прогулках и ограничивают его минимальную физическую активность. Иногда у членов семьи пациента наблюдается тот тип реакции на болезнь родного человека, когда поведение родственников выражается полным отрицанием заболевания у пациента или снижена оценка тяжести перенесенного заболевания. «Золотая середина», которая образуется между двумя типами реакции ближайшего окружения пациента на его заболевание, и есть верная и адекватная реакция семьи на перенесенное заболевание. Также и взаимоотношения между мужем и женой после того, как один из них перенес острый инфаркт миокарда, становятся одним из наиболее значимых психотерапевтических, а иногда психотравматизирующих факторов, поэтому немаловажным условием будет семейная психотерапия. Значимый аспект – социальная реабилитация. Больной после перенесенного инфаркта миокарда является нетрудоспособным 4 месяца, потом пациента направляют на ВТЭК. К этому времени 50% больных возвращается к своей трудовой деятельности, т. е. трудоспособность практически полностью восстанавливается. Если возникают осложнения, то временно присваивается группа инвалидности, чаще всего II, на 6-12 месяцев. Реабилитация в социальном плане – это восстановление социальной деятельности человека как субъекта общественной жизни; в медицинском плане – это ликвидация нарушений здоровья как причины нарушений дееспособности. После перенесенного инфаркта миокарда сроки временной нетрудоспособности (ориентировочные) составляют: при мелкоочаговом инфаркте миокарда, протекающем без осложнений, – приблизительно 2 месяца; при крупноочаговом (в том числе трансму-ральном инфаркте миокарда) – 2–3 месяца; при мелкоочаговом или крупноочаговом осложненном инфаркте миокарда – 3–4 месяца. При рецидивирующем инфаркте миокарда, тяжелых нарушениях ритма и проводимости, выраженной хронической коронарной недостаточности, недостаточности кровообращения ПБ стадии больных направляют на медико-реабилитационную экспертную комиссию, которая или продлевает больничный лист свыше 4 месяцев (если реальна перспектива восстановления трудоспособности), или признает больного нетрудоспособным. При первом функциональном классе больные полностью трудоспособны, но освобождаются от ночных смен, дополнительных работ, командировок. Лица, профессия которых неразрывно связана с тяжелым физическим трудом, переводятся на другую работу. При втором функциональном классе больные трудоспособны, но только в случае, если их работа связана с легким физическим трудом, неинтенсивным физическим напряжением. При третьем функциональном классе больные признаются нетрудоспособными, если их профессия связана с физической нагрузкой и интенсивным психоэмоциональным напряжением. При четвертом функциональном классе больные нетрудоспособны.
Лечение психических нарушений у больных инфарктом миокарда. На первой неделе заболевания возможно развитие острого психоза, что обусловлено интоксикацией продуктами распада некротического очага, гипоксемией и нарушениями мозгового кровообращения. Обычно психозы возникают в вечернее время, протекают с резким двигательным возбуждением, нарушениями сна, у больных развивается тревога, страх, нередко при таких состояниях выявляются зрительные галлюцинации. Для купирования острых психозов рекомендуется внутривенное введение 1–2 мл седуксена (реланиума), 1–2 мл 0,25%-ного раствора дроперидола (под контролем АД). Можно воспользоваться внутримышечным введением 1–2 мл галоперидола, 1 мл аминазина.
| Назад | Оглавление | Далее |