Дети-инвалиды
Основы питания детей с церебральным параличом старше одного года
Значение питания в комплексе реабилитационных мер
Для эффективной реабилитации и абилитации ребенка с ДЦП требуется комплексный подход. Значительную роль в этом комплексе играет питание. От того, что ест ребенок и каким образом происходит кормление, во многом зависит качество его жизни и социализация.
При отсутствии сбалансированной диеты даже взрослый здоровый человек может испытывать дискомфорт, боли, проблемы с весом, дефекацией, настроением. Зачастую возникает хроническая усталость, падает иммунитет. Если же речь идет о ребенке, и тем более – ребенке с серьезными нарушениями развития, то на его физическом и психическом состоянии тем более будет неблагоприятно сказываться дефицит основных нутриентов – витаминов и минеральных веществ, поступающих с пищей.
У детей с ДЦП мышечная спастика или выраженная атония, гиперкинезы, проблемы с жеванием и глотанием пищи, псевдобульбарный, бульбарный синдром, ГЭРБ(Гастроэзофагеальная рефлюксная болезнь.) (с образованием эрозий и рвотами), сниженная физическая активность, сопутствующие заболевания (эпилепсия, частые пневмонии, бронхиты и др.) приводят к быстрому прогрессированию белково-энергетической недостаточности. Также для детей с ДЦП характерны повышенные энергозатраты, связанные с нарушением энергообмена и недостаточной регуляцией функций вегетативной нервной системы.
Понятно, что при таких проблемах физическая абилитация, ежедневно необходимая детям с этими формами ДЦП, становится малорезультативной, так как у ребенка не хватает сил на двигательную активность вследствие нутритивной недостаточности.
О питании детей первого года см.: Лечебное питание детей первого года жизни. (Под ред. А.А. Баранова и В.А. Тутельяна). – М.: Союз педиатров России, 2011; Методические рекомендации о детском церебральном параличе для родителей пациентов. (Под ред. Т.Т. Батышева, главного специалиста по детской неврологии Департамента здравоохранения). – М., 2012.
Основные понятия
Нутритивная недостаточность – это дисбаланс между потребностями организма в питательных веществах и количеством поступающих нутриентов. Это состояние зависит от количества потребляемых питательных веществ, от изменений потребностей организма в питательных веществах, а также усвояемости нутриентов. Нутритивная недостаточность служит прямым показанием к назначению нутритивной поддержки.
Иногда бывает достаточно скорректировать питание, подобрав индивидуальную диету, адекватный путь введения пищи, медикаментозную поддержку. В ряде случаев требуется назначение энтерального или парентерального питания.
Фортификация – обогащение пищи витаминами, микроэлементами.
Индивидуальная диета – диета, назначаемая врачом в соответствии с диагнозом и общим состоянием ребенка. В настоящее время в отдельных случаях с успехом используются такие диеты, как безглютеновая, бесказеиновая и пр. Отсутствие данных доказательной медицины об их клиническом применении не позволяют рекомендовать их в рамках данного методического пособия.
Парентеральное питание – способ введения питательных веществ в организм путем внутривенной инфузии в обход желудочно-кишечного тракта. Может быть частичным и полным. Применяется, когда пациент не может принимать и/или усваивать пищу либо когда есть опасность ухудшения болезни при питании через рот, зонд или стому, а также при невозможности дать достаточное количество нутриентов.
Энтеральное питание (ЭП) – вид клинического питания, при котором доставка в организм пациента питательных веществ в составе лечебных смесей осуществляется внутрижелудочно через желудочный зонд или гастростому или внутрикишечно – через зонд, заведенный в 12-перстную или тонкую кишку; через еюностому. В настоящее время появились лечебные смеси для перорального и энтерального питания (сипингового, то есть маленькими глотками).
Потребность в энтеральном питании зависит от тяжести клинических проявлений основного (ЦП) и сопутствующих заболеваний ребенка, напрямую влияющих на появление питательной недостаточности.
Для назначения ЭП есть прямые показания:
1. Невозможность дать необходимое ребенку количество калорий в пределах максимально возможного по возрасту/росту суточного объема пищи.
2. Гипотрофия 1–4 степени:
• острая, выражающаяся в дефиците массы по росту;
• хроническая, сопровождающаяся существенной задержкой роста.
3. Быстропрогрессирующая потеря массы тела: более 2% за неделю, 5% за месяц, 10% за 3 месяца.
4. Гипопротеинемия, гипоальбуминемия.
5. Отсутствие возможности оптимального естественного питания.
6. Возросшие из-за гиперкатаболизма потребности.
Но есть и абсолютные противопоказания к назначению ЭП:
• органическая и паралитическая непроходимость кишечника;
• кровотечение из ЖКТ;
• неукротимая рецидивирующая рвота;
• острый деструктивный панкреатит;
• анурия.
Безопасность кормления
Прежде чем решать вопрос о нутритивной поддержке, нужно убедиться, что кормление ребенка происходит безопасным для него способом и не вызовет серьезных осложнений. Речь идет, в первую очередь, об аспирации, которая столь часто становится причиной пневмоний и внезапной смерти.
У безопасного кормления есть несколько составляющих. Рассмотрим их подробнее.
Чтобы кормление ребенка было безопасным, нужно:
1) оценить способность ребенка к проглатыванию пищи и напитков;
2) выбрать безопасный метод введения пищи и напитков;
3) в дальнейшем принимать меры для восстановления акта глотания и возвращения к естественному пути приема пищи;
4) следить за правильным положением ребенка при кормлении;
5) соблюдать оптимальный порядок кормления.
1. Оценка акта глотания
Нарушение акта глотания (дисфагия) этиологически связано с тремя причинами: нейрогенной (поражение нервной системы и мышц), психогенной (истерические рвоты, снижение или избирательность аппетита, тревожность – так называемая боязнь первой ложки, нарушение детско-родительских отношений), ятрогенной (последствия оперативных вмешательств, наркоза, наличие трахеостомы).
Дисфагия является последовательной или изолированной дисфункцией оральной, фарингеальной и эзофагальной фаз глотания.
Нарушения на I фазе глотания – оральной. Проблемы проявляются в нарушении формирования пищевого комка. Причинами могут быть нарушения жевания, псевдобульбарный паралич, неугасшие рефлексы новорожденных, сниженный нёбный и глоточный рефлекс.
Жевание – произвольный акт. Помимо возможностиу ребенка должно быть желаниеего осуществлять. Мотивацией жевания является привлекательная пища. Необходимо учитывать присущую большинству детей, в том числе и детям с ЦП, тревожность, связанную с первой пробой незнакомой пищи: нужно стараться заинтересовать, стимулировать ребенка на «эксперимент».
При нарушении этой фазы жевания эффективными являются изменения в консистенции пищи (измельчение), однородности (разделение на жидкую и твердую), месте в полости рта, куда ее кладут (за щеку, на середину языка, на корень и т. д.)
Нарушения на II фазе глотания – фарингеальной. Проблемы проявляются в отсутствии синхронности акта глотания и дыхания. При этих проблемах эффективными могут оказаться изменения в густоте пищи (использование загустителей), ее консистенции (измельчение), однородности (разделение на жидкую и твердую), вкусе, температуре (пища, питье температурой 36° вызывают наибольшие проблемы при нарушении глотания на этой фазе).
Нарушения на III фазе глотания – эзофагальной. Проблемы связаны с состоянием пищевода (последствия операций, стенозы, спайки, эрозии и пр.). Показана консультация гастроэнтеролога, торакального хирурга.
Во время кормления о высокой вероятности дисфагии свидетельствуют следующие признаки:
• кашель или покашливание до, во время или после глотания;
• изменение качества голоса во время или после глотания, например, «влажный», «булькающий» голос, хрипота, временная потеря голоса;
• затрудненное дыхание, прерывистое дыхание после глотания;
• затруднения при жевании;
• слюнотечение или неспособность сглатывать слюну;
• выпадение пищи изо рта во время еды (это может быть следствием того, что у человека плохо смыкаются губы или его язык давит вперед во время глотка вместо нормальных движений вверх и назад);
• срыгивание;
• «смазанная» речь.
Иногда наличие проблемы можно определить лишь косвенно по частым бронхопневмониям или при инструментальном исследовании (так называемые немые аспирации при медленном стекании пищи в дыхательные пути).
О порядке обследования пациента с дисфагией читайте ниже, в разделе «План обследования пациента с дисфагией».
2. Выбор безопасного метода введения пищи и напитков
При дисфагии жизненно важно для больного незамедлительно выбрать альтернативный безопасный метод введения пищи и напитков: питание через зонд или гастростому.
Гастростома – это искусственно созданный канал для кормления или введения лекарств непосредственно в желудок через отверстие (стому) в брюшной стенке. Гастростома используется, когда показания к зондовому кормлению прогнозируемо сохранятся дольше одного-трех месяцев, так как длительное использование назогастрального зонда может привести к развитию осложнений (пролежни, инфекции пазух носа, заброс содержимого желудка в пищевод и легкие, эрозивно-язвенные изменения, желудочное кровотечение).
Виды гастростомических трубок:
• чрескожная эндоскопическая;
• баллонная (длинная и низкопрофильная).
Прямые показания к кормлению через зонд или стому
1. Невозможность приема пищи через рот:
• проблема с глотанием и жеванием;
• отказ от еды.
2. Опасность аспирации.
Гастростомические трубки устанавливается с помощью эндоскопа под защитой наркоза, вся процедура занимает 15–20 минут. Трубки подбираются индивидуально. Преимущество баллонных трубок в том, что наркоз дается, как правило, только один раз – при первичной установке трубки. Замена чрескожной трубки производится при повторной госпитализации и даче наркоза, баллонной – в домашних условиях. Желательная регулярность смены гастростомических трубок – каждые 4–6 месяцев.
Уход за современными гастростомическими трубками прост и удобен. Ребенка с такими трубками можно купать, выкладывать на живот, они не заметны под одеждой и, как правило, не требуют перевязок.
Возможные проблемы – подтекание содержимого желудка, местная инфекция, грануляции, закупорка, выход трубки – обычно решаются в домашних условиях и не требуют госпитализации.
Итак, выбирая альтернативный метод кормления – зонд или гастростому, – нужно учитывать, что назогастральный зонд можно применять не более 1–3 месяцев из-за риска серьезных осложнений (см. выше). Поэтому правильнее будет сразу установить гастростому. Как только необходимость в ней отпадет, ее извлекают, и в кратчайшие сроки отверстие полностью заживляется.
3. Восстановление акта глотания
Если ради безопасности пациента был выбран альтернативный способ кормления, в дальнейшем желательно применять методики восстановления процессов жевания и глотания, используемые логопедами. При успешном применении эти методики могут помочь со временем вернуться к естественному пути приема пищи и напитков, расширить рацион, снизить риск аспирации. Об этом см. в Главе 9 (раздел «Логопедические проблемы и способы их решения»), а также в Главе 7 (раздел «Методика Кастильо Моралеса»).
4. Правильное положение ребенка при кормлении
Для облегчения акта глотания и уменьшения риска аспирации кормить ребенка нужно в максимально возможной вертикальной позе. Идеально – если ребенок при этом сидит на стульчике для кормления или в домашней коляске.
Если вертикализация невозможна, допустимо положение: корпус приподнят (угол 40–45°), голова немного приподнята с помощью валика, плечи приведены вперед (нужны валики под руки), валик под коленями, под стопами упор. Возможно также положение приподнятого корпуса в полуразвороте с сохранением остальных позиций.
В положении сидя должны исключаться рефлексзапрещающие позиции, ведущие к максимальному расслаблению мышц, в том числе мышц, участвующих в глотании. Обычно это положение лежа или на руках ухаживающего. Правильное положение сидя: фиксация таза, установка суставов ног в положение 90–90–90° (тазобедренный–коленный–голеностопный сустав), упор под локти на уровне груди, приведение головы к центральному положению (по средней линии).
Положение на руках является оптимальным только для кормления детей первых месяцев жизни, еще не способных самостоятельно удерживать голову и сидеть.
5. Порядок кормления
Для переваривания пищи важное значение имеет режим, место кормления и некоторые другие факторы. Правильный порядок кормления предполагает максимально возможное участие ребенка в процессе питания. Тогда и процесс пищеварения проходит оптимально.
При использовании зонда или гастростомы порядок кормления зависит от состояния ребенка. Если состояние позволяет, то порядок соблюдается в полном объеме с тем лишь отличием, что питание вводится другим путем. По разрешению врача небольшое количество пищи (1–5 чайных ложек) может предлагаться перорально для поддержания органолептических ощущений и лучшей выработки пищеварительных соков и ферментов.
Кормление ребенка с ЦП через соску можно считать безвредным только до двухлетнего возраста. При более длительном использовании соски происходит задержка рефлексов новорожденных, однообразные длительные иттерационные (повторяющиеся) движения оказывают тормозящее влияние на стволовые структуры, мешают формированию произвольности на корковом уровне.
Порядок кормления(памятка для ухаживающих)
Кормить ребенка нужно в специальном месте в соответствии с назначенным режимом. Недопустимо использовать во время кормления отвлекающие факторы (телевизор, видео и пр.).
1. Предупредить ребенка (даже если считается, что он не понимает обращенную речь), что наступает время поесть, назвать предстоящий прием пищи (завтрак, обед, ужин), сказать, что он будет есть, зачем это нужно (при сниженном аппетите).
2. Перед едой ребенку обязательно вымыть руки, если предполагается хотя бы минимальный их контакт с пищей и столовыми приборами.
3. Переместить ребенка в специальное место для кормления, придать правильное положение сидя или полулежа.
4. Желательно использовать индивидуальный набор посуды с детской тематикой, если ребенок полностью или частично питается через рот.
5. Если состояние ребенка позволяет, при кормлении через рот нужно использовать руку самого ребенка (пассивно, пассивно-активно, активно): это является значимым развивающим фактором.
6. Активно одобрять за количество съеденного, поощрять и заинтересовывать в еде.
7. После кормления вытереть лицо, руки ребенка, при необходимости переменить одежду или постельное белье, убрать посуду, навести порядок.
8. После кормления поддерживать положение ребенка сидя или полулежа в течение 40 минут для уменьшения вероятности рефлюкса и аспирации. В это время в качестве поощрения можно использовать просмотр спокойных, лучше – хорошо известных ребенку телепередач.
При питании через зонд или гастростому без возможности вертикализации ребенок находится в положении полулежа. Из ритуалов остаются обязательными пункты 1, 6, 8.
План обследования пациента с дисфагией
1. Сбор жалоб и анамнестических данных с обязательным уточнением информации об условиях возникновения дисфагии, в том числе о консистенции пищи
Клинический осмотр пациента включает в себя оценку глотания по стандартизированной скрининговой шкале, позволяющей определить способ безопасного кормления и избежать указанных выше осложнений (см. Приложение 7). Осмотр проводится медсестрами.
Высоким признается риск аспирации, если из перечисленных ниже признаков имеются два или более. Низкий уровень – если в наличии только один признак. Если нет ни одного из перечисленный признаков – риск аспирации отсутствует.
Признаки наличия риска аспирации:
• дизартрия (перед началом теста);
• дисфония (перед началом теста);
• аномальный кашель (перед началом теста);
• слабый или отсутствующий рвотный рефлекс (проверяется перед тестом);
• кашель сразу же после проглатывания воды;
• изменение голоса (в течение первой минуты после проглатывания воды просят, если это возможно, сказать «аааа»).
Также в амбулаторной практике для оценки навыков приема пищи и питья можно использовать Международный уровневый опросник EDACS (Eatingand Drinking Ability Classification System). Шкала и алгоритм разработаны Фондом национальной системы здравоохранения Департамента Графства Сассекс (Великобритания). К сожалению, пока у правообладателя не получено разрешение на публикацию опросника на русском языке, но информация о шкале доступна на английском (См.: www.EDACS.org, http://www.sussexcommunity.nhs.uk/downloads/get-involved/research/chailey-research/edacs/edacs-guidelines-translation.pdf (дата обращения: 1.08.2017).
Опросник построен как алгоритм выяснения способности пациента пить и есть (в том числе откусывать и жевать твердую пищу, глотать пищу и жидкость) без риска аспирации. В зависимости от количества и качества ограничений, определяется уровень по шкале – от I, который в еде и питье не отличается от своих обычных сверстников – до V, для которого возможно только зондовое кормление. С возрастанием уровня увеличивается риск осложнений при кормлении через рот (аспирация, потеря веса).
Начиная со II уровня врач должен оценивать сопутствующую клиническую картину:
1) наличие частых (возможно, аспирационной природы) бронхитов и пневмоний;
2) отрицательная динамика веса;
3) возможность употребления ребенком достаточного объема пищи;
4) длительность существующих изменений (во время острого заболевания, в течение нескольких месяцев).
Если нет риска аспирации, решается вопрос о методе нутритивной поддержки.
2. Тест оценки глотания
Если есть риск аспирации, то проводится тест на оценку глотания с продуктами различной плотности и объемом (последовательно) 5, 10 и 20 мл:
• консистенция «нектар» (густой кисель, мед, густая сметана, то есть такая, которая медленно стекает с ложки). Если глотание на этом этапе нарушено, необходимо перейти к тесту с пудингом;
• консистенция «жидкость» (вода, сок, чай, кофе). Если глотание на этом этапе нарушено, необходимо перейти к тесту с пудингом;
• консистенция «пудинг» (пудинг, густой йогурт).
Тест проводит специалист по глотанию – логопед.
Показатели дисфункции глотания (достаточно одного критерия):
• кашель;
• падение SpO2;
• изменение фонации.
Если выявлена дисфункции глотания, в дальнейшем, по возможности, проводится инструментальное исследование, которое оценивается по двум шкалам: по шкале оценки аспирации в соответствии с критериями Rosenbek (Приложение 8) и Федеральной эндоскопической шкале по оценке тяжести дисфагии (Приложение 9).
3. Инструментальные исследования при дисфункции глотания
Фиброларинготрахеоскопия
Это наиболее информативный метод для оценки динамики расстройств глотания. Он позволяет оценить положение надгортанника и объем его движений при глотании, чувствительность слизистой оболочки гортаноглотки и визуализировать затекание слюны в трахею. Фиброскопия позволяет оценить подвижность голосовых складок при дыхании и попытке фонации, оценить объем движения черпаловидных хрящей, качество смыкания голосовой щели при глотании, выявить наличие отека и воспалительных изменений слизистой оболочки гортани, осмотреть подскладочное пространство и оценить проходимость трахеи.
Недостатки метода: аспирацию можно заметить только до и после глотания (во время глотания – «белое пятно»).
Эзофагоскопия
Метод позволяет определить наличие спазма пищевода, механического препятствия пассажу болюса по пищеводу, провести биопсию для цитологического исследования материала на ранней стадии.
Рентгеновское обследование
С его помощью возможно оценить состояние легких, желудка и пищевода. Рентгеновское исследование грудной клетки позволяет оценивать состояние легких (наличие ателектаза нижней доли правого легкого и др.), средостения (уровня жидкости и др.), желудка (отсутствие газового пузыря). Особенно информативно рентгеновское исследование пищевода с глотанием бария (проводится в первые 48 ч после глотания). Асимметричное сужение просвета пищевода с неровными контурами позволяет предположить наличие опухоли, а симметричное, равномерное сужение – диффузный спазм пищевода.
Видеофлюороскопия
Это исследование остается «золотым стандартом» диагностики дисфагии и подбора консистенции пищевых болюсов. Это динамическая флюроскопическая оценка оральной, орально-трансферной, фарингиальной и частично эзофагальной (пищеводной) стадий глотания. Можно выявить аспирацию до, во время и после глотания, позволяет определить локализацию дисфагии, возможную причину (наличие мышечного спазма пищевода).
Недостатки метода:
• радиационное воздействие;
• не видно непосредственно голосовые связки;
• нужен рентгенологический кабинет и некоторая степень мобильности пациента;
• не видно секреции;
• ограничена информация о сенсорном компоненте.
Из-за использования радиоактивных изотопов исследование проводят после рентгеновского, но с перерывом не менее 12 часов. Такого времени достаточно для очищения пищевода от бария.
Оценка нутритивного статуса
1. Оценка физического развития
Чтобы понять, нужна ли ребенку коррекция питания, каков оптимальный алгоритм нутритивной поддержки, нужно оценить гармоничность его развития и, при необходимости, соотношение жировой и мышечной массы.
Как это можно сделать?
Вариант 1. По центильным таблицам для детей от 1 года до 7 лет
К сожалению, в России не существует специальных центильных таблиц для детей с ЦП. Однако, ориентируясь на центильные таблицы ВОЗ по детям с ЦП и зарубежные публикации, можно сделать вывод, что необходимо делать поправку на заболевание и понимать, что отставание этих детей в физическом развитии при отсутствии грамотной коррекции неизбежно прогрессирует с возрастом и напрямую зависит от уровня GMF и выраженности спастики.
Чтобы выяснить, нужна ли коррекция питания ребенка, нужно:
1) оценить физическое развитие ребенка;
2) определить энергозатраты;
3) определить и рассчитать основные нутриенты.
GMF 1: незначительные отклонения от средних (50 центилей) и нижних (10 центилей) весовых показателей в сторону снижения. При небольшом (около 1 кг) отклонении верхнего (90 центилей) в сторону увеличения рост равномерно незначительно отклонен в сторону снижения.
GMF 2: 50 центилей по весу детей с этой группой ЦП примерно соответствуют 10 центилям здоровых; 50 центилей по росту – несколько ниже 10-центильного показателя здоровых детей.
GMF 3: 50 центилей по весу примерно равно 3 центилям здоровых детей; 50 центилей по росту – менее 3 центилей здоровых детей.
GMF 4: 50 центилей по весу примерно на 1 кг ниже 3 центилей здоровых детей; 50 центилей по росту – на 3–4 кг ниже 3 центилей здоровых детей.
GMF 5: нарастание роста и веса замедляется с первых месяцев жизни, а с двух лет вес нарастает в 2 раза медленнее, чем рост. Поэтому массо-ростовой показатель до 7 лет на 2 единицы меньше, чем у здоровых детей. В цифрах это выглядит примерно так: 10-, 50-, 90-центильный массо-ростовой показатель снижен на 2 единицы; снижение ростового показателя нарастает от 1 года до 7 лет от 7 до 18 см разницы по сравнению с показателями здоровых детей соответственно; весового от 1 года до 7 лет – от 2 до 6 кг.
Вариант 2. Вычисление индекса массы тела (ИМТ) у детей старше 7 лет
Расчет индекса массы тела (Кетле II) наиболее информативен для оценки состояния питания детей старше 7 лет. Вычисляется с помощью формулы:
ИМТ = вес (кг) : рост (м)2 (в квадрате)
Результат оценивается следующим образом:
ИМТ = 16 и менее – выраженный дефицит массы;
ИМТ = 16–18 – недостаточная (дефицит) масса тела;
ИМТ = 18–25 – норма;
ИМТ = 25–30 – избыточная масса тела (предожирение);
ИМТ = 30–35 – ожирение первой степени;
ИМТ = 35–40 – ожирение второй степени;
ИМТ = 40 и более – ожирение третьей степени (морбидное).
Норма ИМТ для детей с ЦП в соответствии с группами GMF:
GMF 1: ИМТ = 18–31;
GMF 2: ИМТ = 16–29;
GMF 3: ИМТ = 12,2–24,2;
GMF 4: ИМТ = 12–23;
GMF 5: ИМТ = 12,7–24.
Пример:
Девочка 1,5 года, ЦП. Рост 74 см, вес 5600 г
ИМТ =5,6 : 0,742= 9
Вывод: ИМТ, равный девяти, говорит о выраженном дефиците массы тела. На основании центильной таблицы роста (рост ниже 10 центилей) можно сделать вывод о наличии хронической нутритивной недостаточности.
Оценки индекса массы тела или центильной таблицы достаточно для понимания необходимости назначения дополнительного лечебного питания. Однако можно использовать и более точные оценочные методы.
Вариант 3. Лабораторные методы определения прогностического индекса гипотрофии
В динамике оцениваются показатель альбумина крови, абсолютное количество лимфоцитов, толщина кожной складки над трицепсом (КЖСТ), окружность плеча (ОП) (Окружность плеча изолированно не является значимым показателем, так как помимо мышечной массы включает в себя толщину костей и нервно-сосудистого пучка, что влияет на интерпретацию результатов. В некоторых таблицах вводится поправка на толщину плечевой кости (10 см2 для мужчин и 6,5 см2 для женщин). Однако для детей такая поправка не значима: им необходимо вносить дополнительные коррективы на возраст. Существуют формулы для расчета показателя окружности мышц плеча (ОМП) – этот показатель характеризует состояние мышечной массы (соматического пула белка):
ОМП (см) = ОП (см) – 0,314 х КЖСТ (мм).
Однако эту формулу тоже невозможно применить у детей с ЦП, так как при атрофии в мышцах увеличивается относительное содержание воды, жиров и коллагена. Поэтому у детренированных и истощенных больных расчет по этой формуле дает завышенный результат.)
Калипером замеряется кожно-жировая складка в области трицепса нерабочей руки. Полученная величина считается интегральным показателем состояния жировых депо организма (см. Приложение 6). Сантиметровой лентой измеряется окружность плеча в области того же трицепса.
Измерение толщины кожной складки
1. Найти нужный участок руки (средняя точка между акромиальным отростком лопатки и локтевым отростком локтевой кости). Рука пациента свободно свисает вниз.
2. Оттянуть кожу с подкожной жировой клетчаткой, зажав ткань между большим и указательными пальцами.
3. Наложить штангенциркуль на 1 см дистальнее пальцев на середине расстояния между основанием и вершиной кожной складки.
4. Кожу во время измерения не отпускают.
5. Через 2–3 с измерить толщину складки с точностью до 0,5 мм.
6. Повторить измерения до трех раз, чтобы результаты не отличались более чем на 1,0 мм, а затем определить среднее значение.
Измерение окружности плеча
1. Измерительную ленту наложить горизонтально. Она должна охватывать руку, касаясь кожи, но не сдавливая подлежащие ткани.
2. Измерения следует проводить трижды с точностью до 1 мм, как и при измерениях толщины кожной складки.
Полученные показатели сравнивают со стандартными и определяют степень нарушения питания.
Лабораторные исследования крови
Уровень альбуминов крови отражает длительный дефицит белка в рационе. При таком дефиците белка быстро снижается и трансферрин. По абсолютному содержанию лимфоцитов можно оценить напряженность иммунитета и недостаточное поступление белка (при его недостатке блокируется ДНК в тканях с высокой репликацией, в частности, костном мозге).
Используя данные, полученные при калипометрии, измерении окружности плеча и лабораторных исследованиях, можно рассчитать прогностический индекс гипотрофии (ПИГ) и, как следствие, риск развития осложнений:
ПИГ (%) = 140–1,5 (А) – 1(ОП) – 0,5(КЖСТ) – 20 (Л)
А – альбумин крови, г/л;
ОП – окружность плеча, см;
КЖСТ – толщина складки над трицепсом, мм;
Л – абсолютное количество лимфоцитов, тыс/мкл.
Оценка:
0–20% – эйтрофия;
20–30% – гипотрофия I степени (минимальный риск развития осложнений);
30–50% – гипотрофия II степени (средний риск);
>50% – гипотрофия III степени (высокий риск).
При отсутствии калипера можно определять ПИГ по формуле:
ПИГ (%) = 100–1,5(А) – 1(ОП),
с другими коэффициентами оценки.
Оценка:
0–20% – эйтрофия;
21–30% – гипотрофия I степени (минимальный риск);
31–40% – гипотрофия II степени (средний риск);
>40% – гипотрофия III степени (высокий риск).
2. Определение энергозатрат и основных нутриентов
Чтобы рассчитать дозировки для нутритивной поддержки детей, необходимо определить их энергозатраты. Для этого есть несколько способов.
Вариант 1. Инструментальные методы
1. Непрямая калориметрия – наиболее точный метод, позволяющий определить необходимое пациенту количество калорий, белков, жиров и углеводов на основании анализа выдыхаемого воздуха. Непрямую калориметрию проводят метаболографом с маской-куполом или маской для пациентов со спонтанным дыханием. Исследование выполняется в покое при пассивной и активной нагрузках.
2. Биоимпедансометрия – метод, основанный на измерении биоэлектрического сопротивления тканей биоимпедансным анализатором. С его помощью осуществляют интегральную оценку состава тела по трехкомпонентной модели: 1) анализ жировой массы, тощей массы и общего содержания жидкости в организме, ИМТ; 2) основной обмен веществ (ккал); 3) соотношение ионов натрия и калия в организме. (Англ. lean body mass – внеклеточная масса (соединительная ткань, внеклеточная жидкость) и активная клеточная масса (клетки мышц и органов, нервные клетки).
Вариант 2. По формулам
Основной обмен можно рассчитать индивидуально по формулам, предложенным ВОЗ:
Формулы основного обмена (ЭОО)
М – масса тела, кг.
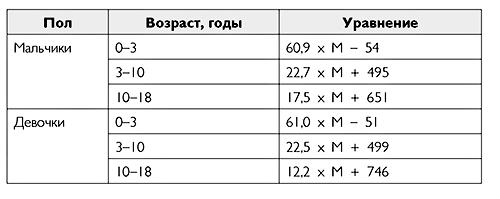
Фактические расходы энергии (ФРЭ)
ФРЭ = ЭОО х ФА х ФС х ТФ х ДМТ.
ФА – фактор активности: постельный режим – 1,3; палатный режим – 1,5; общий режим – 1,7.
ТФ – температура тела: 38–1,1; 39–1,2; 40–1,3; 41–1,4.
ДМТ (дефицит массы тела): 10–20% – 1,1; 20–30% – 1,2; больше 30% – 1,3.
ФС (фактор стресса): отсутствует – 1,0; нетяжелые операции – 1,2; большие операции – 1,3; перитонит – 1,4; сепсис – 1,5; тяжелые травмы – 1,8; сотрясение мозга – 1,9; ожоги до 20% –1,5; ожоги 20–40% – 2,0; более 40% – 2,5.
Приводимые коэффициенты не установлены раз и навсегда, они постоянно пересматриваются специалистами. Так, зачастую на практике диетологи рекомендуют к полученному ФРЭ добавлять 20–30% полученной калорийности, учитывая более высокий расход энергии у детей со спастичными и гиперкинетическими формами ЦП.
Вариант 3. Статистический метод
По неопубликованным данным одного из московских НИИ, регулярно проводящим непрямую калориметрию детям с тяжелыми формами ЦП, у таких детей выявлен повышенный расход энергии вне зависимости от его формы: 70–80 ккал/кг (при средних 18 ккал/кг).
Важно! Для большинства тяжелобольных детей сам прием пищи является существенной физической нагрузкой, если не используются альтернативные пути введения пищи. Это также надо учитывать при вычислении необходимой калорийности (эмпирически).
По общему мнению специалистов, занимающихся проблемами питания детей со спастическими и гиперкинетическими формами ЦП, коррекция нутритивного статуса таких пациентов является практически неразрешимой задачей без применения альтернативных методов введения пищи (то есть кормления через зонд или гастростому).
Без этого детям невозможно дать необходимый объем пищи. При спастике и гиперкинезах организм неспособен воспринять и переварить необходимое (значительно повышенное!) в таких случаях количество калорийной пищи, в том числе и энтерального питания.
3. Расчет основных нутриентов
Корректируя питание, врач всегда должен помнить об опасности превышения нормы по основным нутриентам и производить их расчет.
1. Избыток белков может привести к азотемии и дисфункции печени.
2. Избыток жиров может привести к дефициту кислорода за счет высокой потребности в нем и иммуносупрессии.
3. Избыток углеводов может привести к стеатозу печени, электролитным нарушениям, гипергликемии, осмотической диарее.
Расчет основных нутриентов при энтеральном питании:
Белки (г/сут) = ФРЭ х 0,15: 4 (но не более 2–2,5 г/кг) (примерно 1 г/кг/сут).
Жиры (г/сут) = ФРЭ х 0,3: 9 (примерно 1 г/кг/сут).
Углеводы (г/сут) = ФРЭ х 0,55: 4 (примерно 4 г/кг/сут).
Обычное соотношение – 1:1:4, которое может меняться в зависимости от возраста, физической нагрузки и пр.
Возможен расчет питания по необходимому количеству белка, когда не удается достичь нужной калорийности. Расчет проводится при контроле содержания азота в крови, чтобы избежать избыточного введения белка.
Расчет питания, выбор лечебной смеси
1. Анализ полученных результатов
Для того чтобы рассчитать, какая нутритивная поддержка необходима ребенку, нужно сравнить полученные результаты (рассчитанное количество калорий, белков, жиров, углеводов) с фактически получаемыми. Для этого необходимо взять данные из дневника питания (см. Приложение 7) за 1 день (или средние за 3 дня) и вычислить разницу получаемого ребенком и необходимого калоража, белков, жиров, углеводов. Эта разница и будет составлять количество и состав нутритивной поддержки (калориии, белки, жиры, углеводы). Для удобства расчета количества калорий по дневнику питания можно воспользоваться одним из онлайн калькуляторов расчета калорийности в интернете.
2. Определение максимально возможного объема пищи

Учитывая частое отставание в физическом развитии детей с ЦП, точнее будет ориентироваться не на возраст, а на рост ребенка.
3. Определение количества пищи на один прием
Вариант 1. По усредненным значениям
Суточное количество (при отсутствии иных показаний по состоянию ЖКТ) распределяется между отдельными приемами пищи относительно равномерно: 350–400 г и 400–500 г соответственно возрасту детей.
Вариант 2. Оценка функционального состояния ЖКТ
Если назначенный физиологический объем правильно подобранного лечебного питания подходящей консистенции и температуры, вводимого постепенно (за 2–4 недели) и медленно (за 20–30 минут), ребенком не усваивается (возникают срыгивания, рвоты, вздутия живота и другие проблемы), необходимо оценить состояние желудочно-кишечного тракта, если это не было сделано заранее. Педиатр проводит стандартные обследования и назначает консультацию гастроэнтеролога. Превентивно объем пищи снижают на одно кормление, питание вводят дробно, часто, по 50–150 мл – в зависимости от переносимости. Если обследование показывает необходимость лечения, проводят медикаментозное, а иногда и хирургическое лечение.
Пример:при длительной безрезультативной медикаментозной терапии ГЭР эффективным методом оказывается операция фундопластики, с помощью которой удается надежно избежать обратного заброса пищи в пищевод.
4. Выбор лечебной смеси
Если нет возможности ввести необходимое количество калорий и нутриентов с общим или диетическим столом, ребенку назначается питание энтеральной смесью.
К стандарту качества современной энтеральной смеси относится:
• достаточная калорическая плотность (не менее 1 ккал/мл);
• безлактозная или низколактозная углеводная составляющая;
• низкая вязкость для перманентного введения;
• отсутствие среди побочных реакций опасного стимулирования кишечной моторики;
• информация о генетической модификации при использовании соевых белков;
• ясное указание места производства.
Какие белковые компоненты входят в состав современных смесей для энтерального питания?
1) интактный или цельный белок: казеин, сывороточный, соевый и т. д. (полимерные смеси);
2) гидролизованный белок – пептиды. В состав пептидов входит от 2 до 99 аминокислот (олигомерные, полу-элементные или гидролизованные смеси);
3) свободные аминокислоты (элементные смеси).
Принципы назначения лечебных смесей
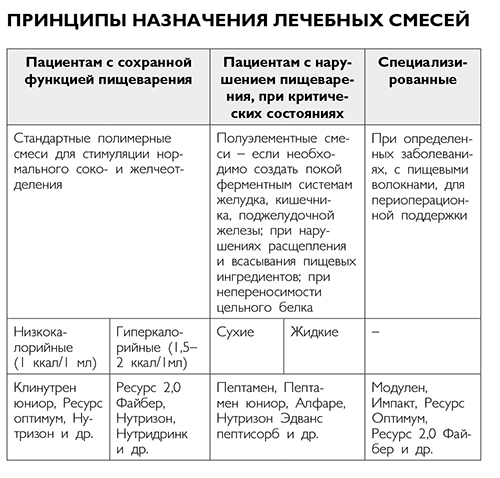
Методы введения смеси для энтерального питания:
• сипинговый – самостоятельный пероральный прием жидкого питания в полном или частичном объеме;
• зондовый (через назогастральный, назоеюнальный зонды);
• через гастростому, еюностому.
Возможные побочные реакции на проведение энтерального питания:
• тошнота, рвота;
• диарея.
Наиболее частые причины побочных реакций:
• неправильное размещение зонда;
• слишком высокая скорость введения смеси;
• выбор концентрации и вида смеси без учета функционального состояния ЖКТ.
Профилактика побочных явлений:
• вводимая смесь должна быть комнатной температуры для перорального введения и подогретая до 37° – при введении в зонд или гастростому;
• вне зависимости от пути введения (перорального, зондового или через гастрому), смесь должна вводиться медленно, с примерной скоростью 100 мл за 10–15 минут.
5. Основные принципы введения лечебных смесей
I. При гипотрофии (нутритивной недостаточности) I степени специализированная смесь при хорошей переносимости вводится за одну неделю.
II. При гипотрофии II степени диетическая коррекция подразделяется на три периода:
1) адаптационный – определение толерантности к пище. Происходит проверка переносимости подобранной смеси, замена ее в случае необходимости;
2) репарационный (промежуточный). Объем питания постепенно (в течение одной недели) увеличивается. В этот период целесообразно назначать ферментные препараты и средства, положительно влияющие на обменные процессы (Р е п а р а ц и я – постепенное увеличение объема питания);
3) период усиленного питания (по произведенному расчету). Ребенок получает рассчитанный объем в комплексе с лекарственными препаратами, улучшающими переваривание и усвоение пищи.
III. При гипотрофии III степени зачастую требуется период стационарного лечения с проведением интенсивной терапии, использованием парентерального питания.
1. Адаптационный период. Энтеральное питание, если оно возможно, оптимально вводить через зонд или гастростому с помощью инфузионного насоса медленно и непрырывно. Длительность этого периода варьирует от нескольких дней до нескольких недель в зависимости от выраженности нарушений толерантности к пище (анорексия, рвота, диарея). Постепенно переходят на порционное введение питательной смеси: 10 раз, затем 7–8 раз в сутки с сохранением и равномерным распределением достигнутого объема. С этой целью можно вначале оставлять постоянную инфузию на ночное время до момента, когда порционное питание по калорийности не превысит 75% дневной нормы потребления.
2. Репарационный период длится 2–4 недели. Целесообразна заместительная ферментотерапия препаратами поджелудочной железы, биопрепаратами. Анаболические средства применяют с осторожностью, так как при их использовании в условиях дефицита питательных веществ возможны глубокие нарушения белкового и других видов обмена, а также угнетение ферментов пристеночного пищеварения. Показано применение витаминотерапии со стимулирующей и заместительной целью. С этого периода начинают лечение сопутствующих заболеваний: рахита, железодефицитной анемии.
3. Период усиленного питания длится от 6 недель.
При гипотрофии основной показатель адекватности диетотерапии – прибавка массы тела. Оптимальной считается прибавка, превышающая 10 г/кг в сутки, средней – 5–10 г и низкой – менее 5 г/кг в сутки.
IV. При эйтрофии лечебная смесь вводится с заместительной или нутриент-корректирующей целью при хорошей переносимости с постепенным увеличением объема за 1 неделю.
V. При гипертрофии с превышением мышечной массы питательная смесь вводится с заместительной или нутриент-корректирующей целью.
Исследования показали, что при переводе детей с гипотрофией на энтеральное питание масса тела повышается преимущественно за счет отложения жира, так как восстановление мышечной ткани без активной работы конечностей невозможно. Таким образом, при отсутствии значительной нагрузки на мышцы из-за спастики и гиперкинезов лечебное питание необходимо сочетать с реабилитационными занятиями, ежедневными дозированными нагрузками.
Необходимые дополнения
Фортификация пищи
У детей с ЦП сопутствующей проблемой, отягощающей состояние, является выраженный дефицит отдельных микроэлементов и витаминов. Причины – недостаток их поступления с пищей или нарушенное усвоение в ЖКТ, недостаток движения, прогулок, прием различных препаратов, в том числе противосудорожных. Известно, что с недостатком кальция, фосфора, витамина Д связаны остеопороз, нарушенный рост зубов; с недостатком железа, фолиевой кислоты – анемия; йода – гипотиреоз и т. д.
Если клиническая картина налицо, педиатр назначает соответствующее лечение.
Иногда дефицит таких значимых элементов, как цинк, магний, селен и прочее остается не диагностированным из-за стертых симптомов. Педиатру может помочь анализ волос пациента на микроэлементы. В отличие от анализа крови, он выявляет хронический дефицит микроэлементов. При своевременной коррекции многих осложнений удается избежать.
Суточный объем воды
Мозг состоит из воды на 60–95%. Многие отделы головного мозга большую часть энергии получают с водой, выступающей в качестве транспортного средства. Недостаточное потребление воды приводит к «сморщиванию» нейронов, замедлению биохимических процессов клеточной коммуникации. Даже легкая дегидратация (1–2%) приводит к значительному снижению когнитивных функций. Также нужно учитывать, что вода участвует в проведении нервных импульсов к различным отделам организма по нейрональной сети. Дисфагия обычно сопровождается де- или гипогидратацией той или иной степени выраженности. Поэтому особое внимание необходимо уделять адекватной гидратации пациентов.
Потребности детей в воде определяются возрастом и массой тела. В России в настоящий момент нет единых рекомендаций по нормам потребления воды детьми.
Самая простая для вычислений формула рассчитывается по массе тела ребенка (для детей старше одного года):
суточный объем воды = 30 мл/кг/сутки.
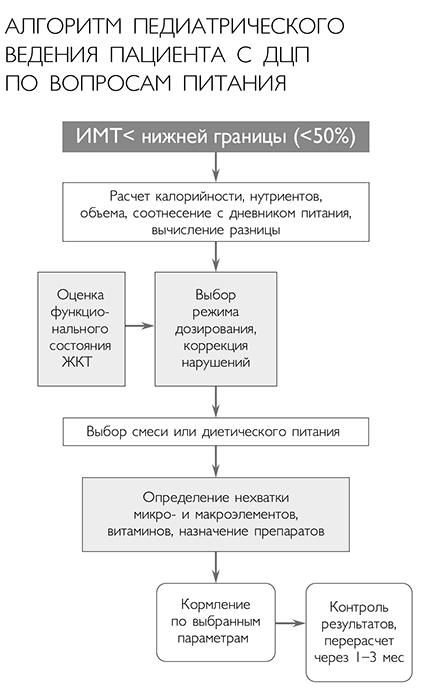
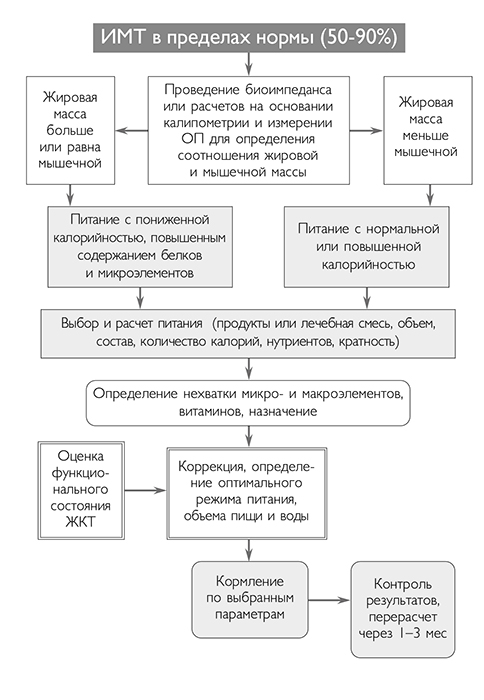
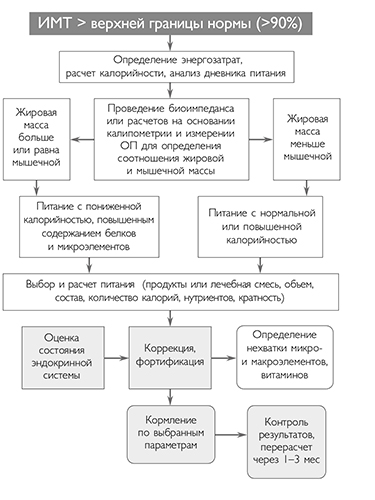
Таким образом, примерный алгоритм ведения пациентов в зависимости от ИМТ после оценки акта глотания и выбора безопасного способа введения пищи можно представить следующим образом (см. схему ниже).
Процесс кормления как социализация ребенка
Процесс кормления, вне зависимости от пути введения пищи, является очень важным моментом в жизни семьи.
Во время кормления происходит взаимодействие ребенка и ухаживающего родственника: дарение и принятие, физический и эмоциональный контакт, порой единственные в течение дня из-за загруженности ухаживающего. Осознавая это, можно использовать кормление и для выражения ребенку своей любви, и для его социализации и развития.
Ребенку нужно давать возможность участвовать в выборе еды, в кормлении (например, пользоваться рукой ребенка с вложенной в нее ложкой, чтобы донести пищу до рта), ощутить консистенцию, температуру пищи не только во рту, но и тактильно. Нужно говорить с ребенком, успокаивать и подбадривать, создавать атмосферу спокойствия и доброжелательности, столь важную и для формирования доверия между ребенком и его близким, и для хорошего усвоения пищи. При отсутствии контакта кормление может стать затруднительным, малорезультативным (потому что полученная пища будет плохо усваиваться, или ее объема будет недостаточно, или повысится риск аспирации) и даже невозможным из-за отказа ребенка.
Алгоритм педиатрического ведения пациента с ДЦП по вопросам питания
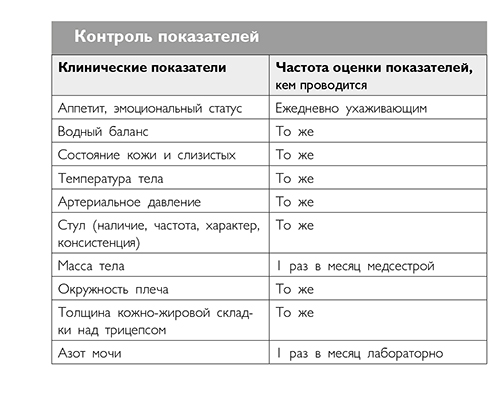
Александра Евгеньевна Коршикова-Морозова, врач-педиатр, паллиативный врач детской выездной службы Марфо-Мариинского медицинского центра «Милосердие» (Москва)
| Назад | Оглавление | Далее |